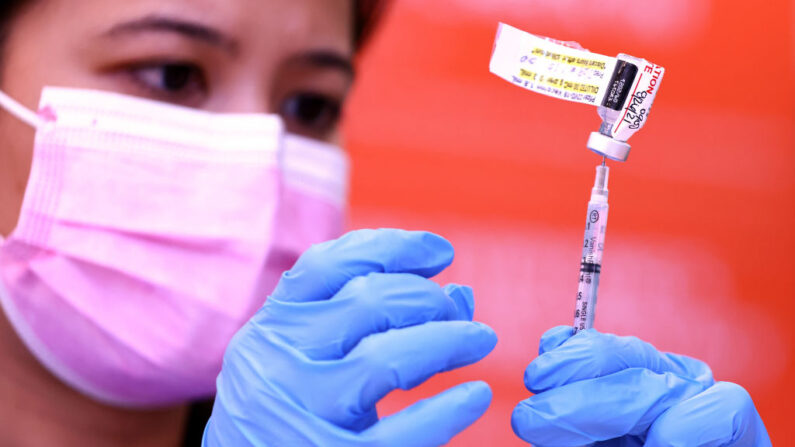
La vacuna contra el COVID-19 de Pfizer y BioNTech, aprobada por la Administración de Alimentos y Medicamentos (FDA) de Estados Unidos, no debe recetarse fuera de lo indicado en la etiqueta, para niños menores de 12 años, ya que no existen datos sobre la dosis adecuada o la seguridad de su uso en los niños, dijo el lunes un funcionario de la FDA.
La comisionada interina de la FDA, la doctora Janet Woodcock, dijo a los periodistas que la agencia federal no cree que sea apropiado que los niños menores de 12 años reciban la vacuna, diciendo que «sería una gran preocupación que la gente vacune a los niños porque no tenemos los datos adecuados».
«No tenemos los datos de seguridad, ni tampoco tenemos todos los datos de eficacia», dijo Woodcock. «Nosotros no estamos recomendando que los niños menores de 12 años sean vacunados con esta vacuna. No sería apropiado».
Las vacunas anti COVID-19 no están disponibles actualmente para niños menores de 12 años en Estados Unidos. Sin embargo, Pfizer dijo en un comunicado en junio que estaba empezando a probar su vacuna de ARNm en un grupo más grande de niños menores de 12 años después de seleccionar una dosis más baja para la inyección en una etapa inicial del ensayo.
Un portavoz de Pfizer dijo a continuación que la empresa espera obtener datos de niños de 5 a 11 años en septiembre y que probablemente solicitaría a los reguladores una autorización de uso de emergencia más adelante ese mes. Los datos de los niños de 2 a 5 años podrían llegar poco después, dijo el portavoz.
La empresa también dijo que está probando una dosis en niños de entre 6 meses y 2 años, y espera tener esos datos en algún momento de octubre o noviembre.
La Academia Americana de Pediatría (AAP), que representa a los médicos de niños, publicó una declaración en la que se hace eco de las observaciones de Woodcock, poco después de que el organismo regulador de medicamentos de Estados Unidos aprobara la vacuna COVID-19 de Pfizer para personas de 16 años o más el 23 de agosto.
«Los ensayos clínicos de la vacuna COVID-19 en niños de 11 años o menos están en marcha, y necesitamos ver los datos de esos estudios antes de administrar esta vacuna a niños más pequeños», dijo el presidente de la AAP, Lee Savio Beers, en una declaración. «La dosis puede ser diferente para edades más tempranas». La AAP recomienda no administrar la vacuna a niños menores de 12 (años) hasta que la FDA lo autorice».
La vacuna fue autorizada para su uso en niños desde los 12 años en Europa y Canadá. Ellos reciben la misma dosis que los adultos: 30 microgramos.
Esto se produce en un momento en que los científicos de Estados Unidos y de otros países están estudiando la posibilidad de una relación entre la inflamación del corazón y las vacunas de ARNm, especialmente entre los varones de 12 a 24 años. Tanto las vacunas de Pfizer como las de Moderna son vacunas de ARNm.
El mes pasado, el comité de seguridad de la Agencia Europea del Medicamento (EMA) concluyó que la inflamación del corazón «puede producirse en casos muy raros» y recomendó «incluir la miocarditis y la pericarditis como nuevos efectos secundarios en la información sobre el producto de estas vacunas, junto con una advertencia para poner en conocimiento a los profesionales sanitarios y a las personas que toman estas vacunas».
El comité asesor de los Centros para el Control y la Prevención de Enfermedades (CDC) mantiene que los riesgos de la inflamación elevada no superan los beneficios de la vacuna y sigue recomendándola a los niños a partir de los 12 años.
Algunos expertos científicos cuestionaron la conveniencia de administrar la vacuna COVID-19 a determinados grupos de personas.
El inventor de la tecnología de la vacuna de ARNm, el Dr. Robert Malone, dijo que la relación riesgo-beneficio de la vacuna para los niños no «parece tan buena».
«Normalmente, el Comité Asesor sobre Prácticas de Inmunización [ACIP] de los CDC evaluaría la relación riesgo-beneficio de una nueva vacuna de forma rigurosa, utilizando años de vida ajustados a la calidad», dijo Malone en el programa American Thought Leaders de The Epoch Times, en julio.
«Entonces el ACIP daría una recomendación diciendo que esta vacuna es buena para ser usada en los ancianos. En este caso, es bastante convincente que, aunque se produzcan efectos adversos, su riesgo [en los ancianos] de muerte o de una enfermedad significativa es bastante alto. Así que es fácil decir que sí».
«Los adolescentes, en cambio, tienen una probabilidad muy, muy baja de enfermedad o muerte por COVID (…) Ese cálculo aquí no sale tan bien parado», indicó Malone.
El presidente Joe Biden dijo a través de una declaración el lunes que la autorización de la FDA para la vacuna de Pfizer «debería dar una mayor confianza en que esta vacuna es segura y eficaz».
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.