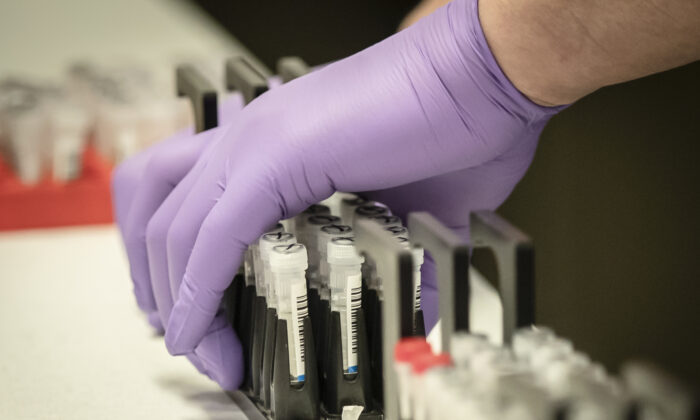
La Administración de Alimentos y Medicamentos (FDA) ha otorgado una nueva autorización de emergencia para una prueba de detección del nuevo coronavirus, la última medida para tratar de ampliar rápidamente la disponibilidad de pruebas en Estados Unidos.
La prueba, desarrollada por Roche, con sede en Suiza, está diseñada para usarse en dos máquinas desarrolladas por la compañía y que están ampliamente disponibles en todo Estados Unidos. Es solo la tercera prueba de coronavirus que recibe una autorización de uso de emergencia por la FDA.
La FDA previamente otorgó la autorización a los Centros para el Control y la Prevención de Enfermedades (CDC), pero la prueba que desarrolló la agencia no siempre produjo resultados concluyentes, lo que llevó a un retraso de semanas en las pruebas del nuevo virus. Recientemente, la FDA otorgó la autorización para una prueba creada por el Departamento de Salud del Estado de Nueva York.
La prueba de Roche proporciona resultados en solo tres horas y media. Al ejecutar pruebas simultáneamente, su mejor sistema puede analizar 4128 resultados en 24 horas, dijo la compañía en un correo electrónico a The Epoch Times.
«Estamos trabajando las 24 horas para aumentar esa cantidad, ya que reconocemos la importancia de que los pacientes accedan a estas pruebas críticas», dijo.

El kit permite a los hospitales y laboratorios realizar pruebas. Millones de pruebas al mes estarán disponibles para las instituciones. El kit analiza muestras tomadas de la nariz o la garganta.
“Proporcionar capacidades de prueba de gran volumen y calidad nos permitirá responder de manera efectiva a lo que la Organización Mundial de la Salud (OMS) ha caracterizado como una pandemia. Es importante detectar de manera rápida y confiable si un paciente está infectado con SARS-CoV-2”, dijo en un comunicado, Thomas Schinecker, CEO de Roche Diagnostics.
Scott Gottlieb, excomisionado de la FDA, dijo que la aprobación del kit de Roche fue «muy significativa».
El nuevo desarrollo «aumentará sustancialmente la capacidad para hacer pruebas a los pacientes, para finales de la próxima semana, en decenas de miles por día en todos los laboratorios, comerciales y académicos», dijo en un comunicado.
Si bien los sistemas de Roche se producen en Suiza, la prueba se está produciendo en Branchburg, Nueva Jersey, en Estados Unidos.

La autorización de uso de emergencia de la FDA permite a las empresas operar fuera de los procesos normales de aprobación.
«Es razonable creer que los beneficios conocidos y potenciales de la prueba autorizada superan los riesgos conocidos y potenciales de dicho producto», dijo Denise Hinton, científica jefe de la FDA, en una carta a Roche.
Los laboratorios de salud pública en los 50 estados ahora están haciendo pruebas de COVID-19, la enfermedad que causa el nuevo virus. Hasta el 12 de marzo, se analizaron más de 13,000 muestras, según los CDC.
Otras compañías también están trabajando en el desarrollo de pruebas para el nuevo virus, mientras que algunas, incluyendo Quest Diagnostics, ya tienen una autorización de uso de emergencia pendiente.
Sigue a Zachary en Twitter: @zackstieber
Le puede interesar
Mamá comparte el secreto que liberó a su hijo del autismo
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.