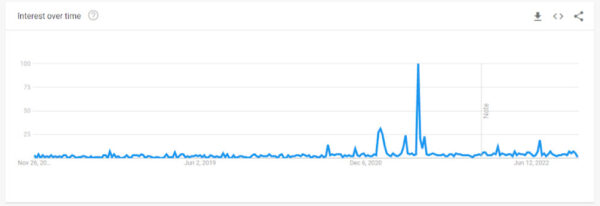
A finales de enero del 2021, justo un mes después de que la Administración de Alimentos y Medicamentos (FDA) concediera la Autorización de Uso de Emergencia (EUA) a las vacunas COVID-19 de Pfizer y Moderna en diciembre del 2020, se hizo evidente un cambio drástico en las búsquedas de tendencias en Google sobre «molde decidual».
Otro aumento del interés se produjo a mediados de junio del 2021, un mes después de que se concediera a la vacuna de Pfizer una EUA ampliada para adolescentes de entre 12 y 15 años.
Un molde decidual se define como: «una pieza grande e intacta de tejido que pasa a través de la vagina en una sola pieza sólida. Ocurre cuando el grueso revestimiento mucoso del útero, llamado decidua, se desprende en la forma casi exacta de una cavidad uterina, creando un molde triangular».
Las mujeres empezaron a denunciar en las redes sociales problemas menstruales inusuales, como el desprendimiento de decidua. Esto dio lugar a varias encuestas en Internet, una de las cuales fue realizada por MyCycleStory.com.
Aunque la bibliografía solo contiene informes de casos de DCS, lo que dificulta la medición de la prevalencia real, se cree que la afección es bastante rara. Se publicaron menos de 40 casos a lo largo de 100 años, normalmente relacionados con embarazos ectópicos, abortos espontáneos o uso prolongado de progesterona.
Sin embargo, 292 mujeres declararon haber experimentado DCS durante un periodo de estudio de MyCycleStory de 7,5 meses en 2021.
Aunque el número absoluto de casos no es tan elevado, este aumento inusual de la incidencia con respecto a la tasa de fondo requiere más estudios para determinar la causa y cualquier otro posible factor relacionado con la pandemia.
Estudios observan un impacto en el ciclo menstrual de las mujeres
En el Sistema de Notificación de Efectos Adversos de las Vacunas (VAERS) de los Estados Unidos, más de 11,000 personas notificaron al sistema un problema relacionado con la menstruación tras la vacunación con COVID-19 en abril del 2022. Los eventos incluyeron sangrado abundante, menstruación irregular o retrasada, oligomenorrea y amenorrea.
Asimismo, el sistema de vigilancia de la tarjeta amarilla de la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del Reino Unido recibió 51,695 notificaciones de trastornos menstruales, incluidas menstruaciones más abundantes o retrasadas y hemorragias inesperadas, tras la vacuna COVID-19.
Los resultados de estas bases de datos sugirieron la posibilidad de impactos negativos en los ciclos menstruales tras la vacunación con COVID-19. La relación entre la vacunación con COVID-19 y el ciclo menstrual se evaluó en varios estudios revisados por expertos.
En un gran estudio prospectivo de cohortes realizado por Harvard, el estudio Apple Women’s Health, se realizó un seguimiento manual de la duración del ciclo de 9682 mujeres vacunadas y no vacunadas que aportaron 128,094 ciclos menstruales, la mayoría de las cuales fueron vacunadas (88 por ciento) con Pfizer (55 por ciento) o Moderna (37 por ciento). Se realizó un seguimiento prospectivo tanto de la duración del ciclo como de la duración de la menstruación para obtener medidas de referencia, vacunación y seguimiento.
Este estudio descubrió que la duración media del ciclo sí aumentaba tras la vacunación, especialmente en el caso de las mujeres que recibían la vacuna durante las dos primeras semanas del ciclo, en la fase folicular.
Tras la primera dosis en la fase folicular, la duración del ciclo aumentó en 0,97 días, y tras la segunda dosis en 1,43 días. El ciclo siguió siendo más largo durante uno o dos meses después de la vacunación y luego volvió a la línea de base.
Las mujeres vacunadas durante la fase lútea tendieron a tener un ciclo más corto (-0,97 días).
Otro estudio prospectivo de cohortes realizado en Estados Unidos con casi 4000 mujeres de entre 18 y 45 años evaluó a las que tenían ciclos de duración normal durante tres ciclos consecutivos antes de la primera dosis de vacuna y tres ciclos después de la vacuna (ciclos 4, 5 y 6). Las no vacunadas fueron evaluadas a lo largo de seis ciclos durante un periodo de tiempo similar.
Los investigadores calcularon los cambios intraindividuales en la duración del ciclo y de la menstruación para los ciclos 1-3 y 4-6 y, a continuación, utilizaron modelos de efectos mixtos para comparar las diferencias en la duración del ciclo y de la menstruación entre las cohortes vacunadas y no vacunadas.
Los investigadores hallaron un aumento medio de 0,91 días en la duración media del ciclo para las mujeres que recibieron la vacuna de ARNm durante su segundo ciclo de vacunación.
Más receptoras de la vacuna tuvieron un cambio en la duración del ciclo de al menos 8 días que las no vacunadas (6,5 por ciento frente a 4,6 por ciento, p=0,017). Los ciclos de vacunación más largos parecían concentrarse entre las 358 personas que recibieron ambas dosis dentro de un mismo ciclo.
En este subgrupo de mujeres vacunadas, el aumento medio no ajustado de la duración del ciclo fue de 2,38 días y una proporción sustancialmente mayor (10,6 por ciento) tuvo un aumento de la duración del ciclo de al menos 8 días en comparación con la cohorte no vacunada (4,3 por ciento, P<0,001).
Los autores no hallaron diferencias en la duración de la menstruación entre las cohortes.
Un estudio más pequeño realizado en Israel entre 219 mujeres que seguían regularmente sus ciclos también halló cambios en la menstruación en casi el 40 por ciento de las mujeres vacunadas. La paridad (número de embarazos) y el uso de medicamentos parecían ser factores de riesgo de irregularidades menstruales.
La mitad de las que sufrían hemorragias irregulares eran multíparas, frente al 31,5 por ciento de multíparas entre las mujeres sin hemorragias irregulares. La presencia de comorbilidades también era mayor entre las mujeres que declaraban sangrados irregulares.
Curiosamente, las mujeres que declaraban tomar medicación con regularidad tenían menos probabilidades de presentar hemorragias irregulares.
Otro estudio incluyó una cohorte prospectiva de 79 mujeres y una cohorte retrospectiva de 1273 mujeres.
En el estudio también se observó un aumento de la duración del ciclo (retraso hasta la siguiente menstruación) en las mujeres que menstruaban espontáneamente, lo que sugiere que la vacunación con COVID-19 puede alargar el ciclo menstrual.
Sin embargo, no se observó tal cambio entre las que utilizaban anticonceptivos, lo que sugiere que este efecto de la vacunación con COVID-19 puede estar mediado por las hormonas ováricas.
Aunque varios estudios (referencias 9-14) sugieren que la infección por COVID-19 puede provocar cambios en la duración del ciclo, el Nurses’ Health Study no detectó tal asociación tras la infección por COVID-19.
En este estudio, la vacunación con COVID-19 se asoció con la duración del ciclo a corto plazo (dentro de los 6 meses posteriores a la vacunación), en particular entre las mujeres con ciclos cortos, largos o irregulares antes de la vacunación. Se detectaron cambios en la duración del ciclo tanto para las vacunas con ARNm como para las vacunas vectorizadas con adenovirus.
Parece razonable que exista una relación plausible entre la vacunación con COVID-19, tanto con vacunas de ARNm como con vacunas vectorizadas con adenovirus, y el aumento de la duración del ciclo. El efecto parece más pronunciado entre las mujeres que ya tuvieron un hijo y que reciben ambas dosis en un solo ciclo, lo que concuerda con el estudio de Israel.
Datos del VAERS sugieren un mayor riesgo de irregularidades en la menstruación y el embarazo
Un estudio preliminar de los acontecimientos adversos (AA) notificados al Sistema de Notificación de Acontecimientos Adversos a las Vacunas (VAERS) comparó la proporción de AA debidos a las vacunas COVID-19 con las vacunas antigripales. Thorp y sus colegas recopilaron datos sobre irregularidades en el embarazo y la menstruación notificadas al VAERS entre el 1 de enero de 1998 y el 30 de junio del 2022.
La proporción de notificaciones de EA relacionados con las vacunas COVID-19 en comparación con las vacunas antigripales fue al menos el doble (y estadísticamente significativa a p<0,05) para lo siguiente:
-Anomalía menstrual (AM), aborto espontáneo (A), malformación fetal (MF), trastornos cardíacos fetales (TCD), anomalías del crecimiento fetal (AGF), vigilancia anormal del feto (SAF), muerte fetal/parto muerto (MF) y bajo nivel de líquido amniótico (BA), que se enumeran en el siguiente gráfico.
Un valor superior a 1 implica que los EA se notifican con mayor frecuencia con la vacuna COVID-19 en comparación con las vacunas antigripales.
-Anomalías cromosómicas fetales, higroma quístico fetal, arritmia fetal, parada cardiaca fetal, mala perfusión vascular fetal, trombosis placentaria fetal, que no se incluyen en el gráfico pero que también aumentaron significativamente.
Debe tenerse en cuenta que, para cualquier estudio VAERS, se trata de un sistema de notificación pasiva que se basa en la notificación de los médicos y puede no reflejar la tasa real de EA. La detección de los EA puede variar significativamente en función del conocimiento público del EA, por lo que la sensibilidad puede ser tan baja como el 1 por ciento de todos los EA o el 67 por ciento. Los autoinformes de los pacientes no están necesariamente confirmados por un diagnóstico médico. La base de datos VAERS es apropiada para la generación de hipótesis, pero se necesitan estudios basados en la población para comprender la verdadera incidencia y causalidad.
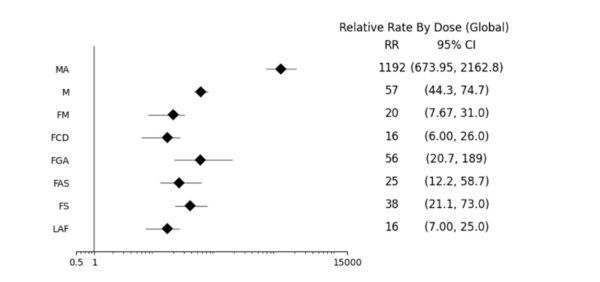
Tasas relativas globales de notificaciones de EA tras vacunas COVID-19 frente a las de vacunas antigripales por dosis administrada.
Fuente de la preimpresión: James A. Thorp, Claire Rogers, Michael P. Deskevich, Stewart Tankersley, Albert Benavides, Megan D. Redshaw y Peter A. McCullough. Vacunas COVID-19: El impacto en los resultados del embarazo y la función menstrual. Enlace de la preimpresión.
Estudio canadiense observó un aumento del riesgo de acontecimientos adversos graves durante el embarazo
Un estudio de cohortes observacional prospectivo canadiense de las vacunas COVID-19, publicado en Lancet Infectious Disease pregnancy,, evaluó la frecuencia de eventos significativos de salud entre 5625 embarazadas / vacunados, en comparación con 339 embarazadas / no vacunados y 185 735 no embarazadas / vacunados controles, lo que resulta un total de 191,360 mujeres de edades 15-49 años incluidos.
Los datos se recopilaron mediante una encuesta con llamadas telefónicas de seguimiento a quienes informaron de algún acontecimiento médico.
Las mujeres embarazadas vacunadas presentaban un riesgo 4,4 veces mayor (IC del 95 por ciento: 2,4-8,3) de sufrir un acontecimiento sanitario grave después de la dosis dos de Moderna, en comparación con las mujeres embarazadas no vacunadas; esta asociación no se observó en las vacunadas con Pfizer.
La dosis de la vacuna Moderna (100 mcg) es más de 3 veces superior a la de Pfizer (30 mcg) en adultos, lo que bien puede explicar los diferentes resultados entre las marcas de vacunas.
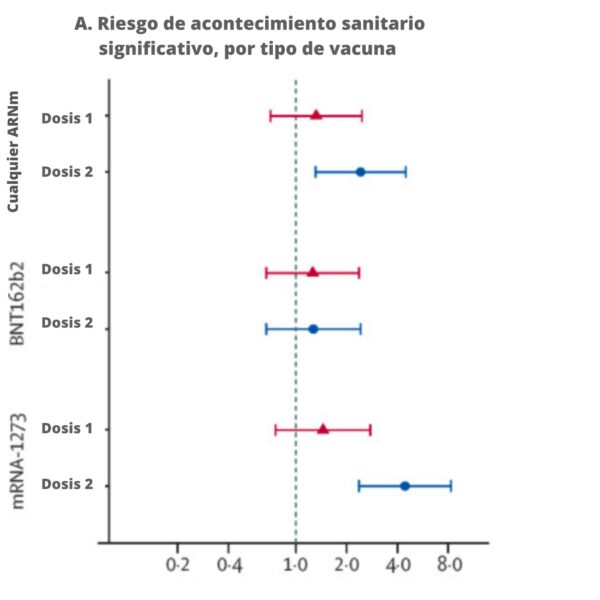
Sadarangani M, Soe P, Shulha HP, Valiquette L, Vanderkooi OG, Kellner JD, Muller MP, Top KA, Isenor JE, McGeer A, Irvine M, De Serres G, Marty K, Bettinger JA; Red canadiense de investigación sobre inmunización. Safety of COVID-19 vaccines in pregnancy: a Canadian National Vaccine Safety (CANVAS) network cohort study. Lancet Infect Dis. 2022 Nov;22(11):1553-1564. doi: 10.1016/S1473-3099(22)00426-1.
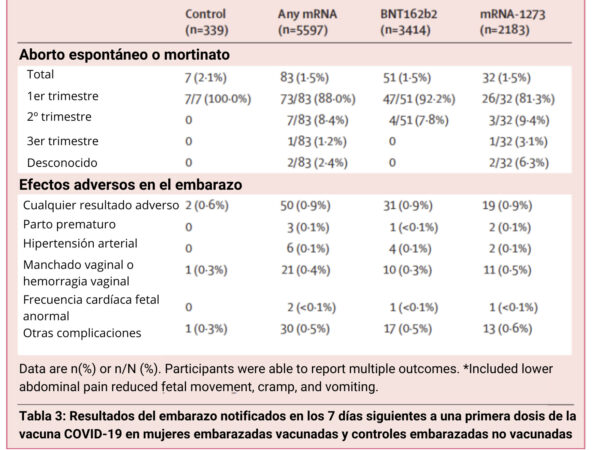
El aborto espontáneo o la muerte fetal fue el resultado adverso del embarazo notificado con más frecuencia. Tanto el aborto espontáneo como la muerte fetal describen la pérdida del embarazo, pero difieren según el momento en que se produce la pérdida. En Estados Unidos, un aborto espontáneo suele definirse como la pérdida de un bebé antes de la semana 20 de embarazo, y un mortinato es la pérdida de un bebé a las 20 semanas de embarazo o después.
Se notificó en tasas similares entre los grupos de control (2,1 por ciento de 339) y vacunados en los siete días siguientes a la dosis uno de cualquier vacuna ARNm (1,5 por ciento de 5.597).
Otros resultados adversos raros del embarazo como hemorragia vaginal, frecuencia cardiaca fetal anormal y movimiento fetal reducido aumentaron ligeramente en los siete días siguientes a cualquier vacunación con ARNm en comparación con el control.
Hubo un número adicional de personas que declararon haber sufrido abortos espontáneos o mortinatos entre la primera dosis de la vacuna COVID-19 y la finalización de la segunda encuesta (dosis dos) (hasta 10 días después de la dosis dos); sin embargo, se desconocía el momento exacto de estos acontecimientos en relación con la vacunación.
Impacto en la fertilidad
El impacto de la vacunación y la infección sobre la función ovárica y la fertilidad es un tema de gran peso. A continuación se resumen las principales conclusiones extraídas de una serie de publicaciones y preprints revisados por expertos.
Reducción de la tasa global de fertilidad (TGF)
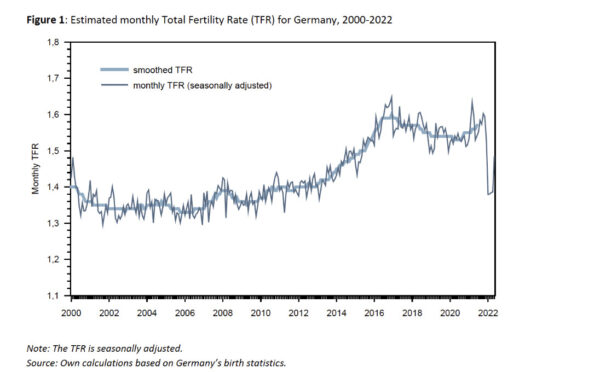
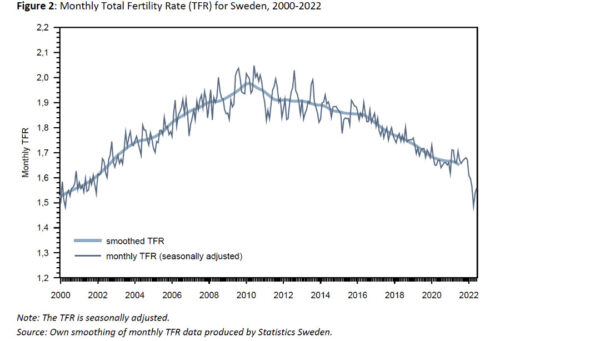
Tras las campañas de vacunación se produce un cambio en la fertilidad de toda la población. En un nuevo preimpreso, se analizaron las tendencias de la tasa global de fecundidad (TGF) en Suecia y Alemania a lo largo del tiempo, desde el inicio de la pandemia hasta 2022.
Muchos países notaron un descenso de la fecundidad al principio de la pandemia, pero Alemania y Suecia no se vieron afectados. Sin embargo, estos países han experimentado recientemente una reducción de la TGF.
La TGF ajustada estacionalmente en Alemania descendió un 14 por ciento pasando de 1,5-1,6 en 2021 a 1,3-1,4 a principios de 2022. Una tendencia similar se observó en Suecia, con un descenso del 10 por ciento, de 1,7 a 1,5-1,6.
Los autores señalan que los fuertes descensos de la TGF coinciden con el inicio de las campañas de vacunación precisamente nueve meses antes. Los autores especulan con que la preocupación por la seguridad de la vacuna durante la concepción y el embarazo podría haber hecho que las mujeres pospusieran la formación de su familia hasta después de la vacunación.
Son necesarias más investigaciones longitudinales basadas en la población para detectar cualquier efecto leve pero significativo de la vacunación sobre la fertilidad.
Tasas de embarazo
Una revisión sistemática y un metaanálisis evaluaron el impacto de las vacunas COVID-19 en la fertilidad
En la revisión sistemática se incluyeron 29 estudios realizados en Israel, Estados Unidos, Rusia, China, Italia, Norteamérica y Turquía.
Se observó que las tasas de embarazo disminuyeron en el grupo vacunado en un 15 por ciento para la tasa de embarazo bioquímica y en un 4,3 por ciento para la tasa de embarazo clínica, en comparación con el grupo no vacunado.
Se informa de que ambos descensos no alcanzaron una diferencia estadística entre los grupos vacunados y no vacunados. Sin embargo, un descenso clínicamente significativo no tiene por qué serlo estadísticamente. Y el hecho de alcanzar o no una diferencia estadística puede estar condicionado por la potencia de los estudios.
Además, se realizaron metaanálisis de la motilidad progresiva de los espermatozoides antes y después de la vacunación (44 por ciento frente a 43 por ciento, p = 0,07).
Hormona antimülleriana (HAM)
La hormona antimülleriana (HAM) se utilizó como marcador para evaluar la función ovárica en las mujeres y su impacto en la fertilidad. Proporciona una estimación de la reserva ovárica, es decir, cuántos óvulos quedan en los ovarios. Las mujeres mayores suelen tener niveles más bajos que las jóvenes.
En un estudio prospectivo realizado en Israel entre 129 mujeres que recibieron dos vacunas de ARNm, se evaluó el cambio en la HAM mediante mediciones basales y a los 90 días, antes y después de la vacunación.
En este estudio, no se detectaron cambios en los niveles de HAM antes y después de la vacunación (5,3 frente a 5,3 µg/l, respectivamente).
Los autores concluyeron que, aunque este estudio se limitaba a un seguimiento de tres meses después de la primera vacunación, no parecía haber ningún efecto de la vacunación con ARNm sobre la función ovárica.
Otro estudio prospectivo israelí similar, aunque más pequeño, entre 31 mujeres sometidas a tratamiento de fecundación in vitro (FIV) descubrió que la HAM permanecía estable antes y después de la vacunación con ARNm.
Los estudios sobre la AMH presentan algunas limitaciones. En primer lugar, no existe un grupo de control y solo se utilizó el autocontrol.
En segundo lugar, se sabe que los niveles séricos de HAM se ven afectados por múltiples factores, como la obesidad, los niveles de vitamina D, las terapias anticonceptivas orales, los genes (mutaciones BRCA que contribuyen a los cánceres de mama y ovario), la quimioterapia, los trastornos ovulatorios comunes (síndrome de ovario poliquístico, SOP) y los antecedentes de cirugía ovárica. Cualquier cambio potencial en los factores de confusión comunes para los niveles séricos de AMF (peso corporal, anticonceptivos, niveles de vitamina D) en estos sujetos debe ser analizado e informado.
En un estudio retrospectivo que incluyó a 200 mujeres sometidas a FIV, no se detectaron diferencias en los resultados de fertilidad, incluidas la recuperación de ovocitos, las tasas de fertilización y embarazo y la calidad embrionaria.
Aunque este estudio halló tasas de embarazo similares entre vacunadas y no vacunadas (32,8 por ciento y 33,1 por ciento, respectivamente), habría sido necesario un tamaño de muestra mucho mayor para detectar una diferencia pequeña pero significativa.
Se necesitaría una muestra de al menos 985 participantes para detectar una diferencia menor del 5 por ciento en las tasas de embarazo. En otras palabras, este estudio no tenía potencia suficiente para detectar una diferencia significativa de reducción en las tasas de embarazo.
En otro estudio de cohortes retrospectivo de 222 mujeres vacunadas y 983 no vacunadas que se sometieron a hiperestimulación ovárica, no se encontró ningún efecto de la vacunación en el resultado primario, la tasa de fertilización, ni en ninguno de los resultados secundarios, incluidos los óvulos recuperados, los ovocitos maduros recuperados, la proporción de ovocitos maduros, la tasa de blastulación o la tasa de euploidía.
En 214 mujeres vacunadas y 733 no vacunadas sometidas a transferencia de euploides congelados descongelados, el análisis ajustado no halló ninguna asociación significativa entre la vacunación y el resultado primario, el embarazo clínico (odds ratio ajustado [aOR] 0,79; IC del 95%: 0,54-1,16), ni ninguno de los resultados secundarios: embarazo (aOR 0,88; IC del 95%: 0,58-1,33), embarazo en curso (aOR 0,90; IC del 95%: 0,61-1,31), pérdida bioquímica del embarazo (aOR 1,21; IC del 95%: 0,69-2,14) o pérdida clínica del embarazo (aOR 1,02; IC del 95%: 0,51-2,06).
Sin embargo, estos intervalos de confianza son amplios y el tamaño de la muestra insuficiente para descartar una diferencia pequeña pero clínicamente significativa en los resultados.
Un pequeño estudio de cohortes de 32 individuos (9 recuperados SARS-CoV-2 positivos, 9 vacunados, 14 no infectados/no vacunados) no encontró diferencias en la función folicular ni en la calidad de los ovocitos.
En conjunto, estos estudios sugieren que cualquier efecto de la infección o de la vacunación sobre la fertilidad será difícil de detectar a menos que los estudios se diseñen con suficiente potencia estadística orientada a los cambios esperados en los criterios de valoración primarios y secundarios.
Una disminución del 0,3 por ciento en el grupo vacunado equivale a 30 embarazos menos por cada 10,000 mujeres, por lo que cualquier estudio diseñado para detectar una diferencia tan leve necesitaría inscribir a 770,000 mujeres.
Algunos podrían sugerir que es poco práctico potenciar los ensayos clínicos de fase III para detectar el impacto en la fertilidad, pero sin duda es posible una vigilancia intencionada posterior a la comercialización cuando la aceptación de la vacuna se cuenta por millones.
Mecanismo de acción de los EA en la salud reproductiva
Se debatieron varios mecanismos moleculares de acción que pueden contribuir a los EA observados en las mujeres.
En primer lugar, la activación inmunitaria tras la exposición a la proteína de la espiga después de la vacunación podría desencadenar una respuesta inmunitaria innata anormal, activar citoquinas inflamatorias y genes inflamatorios.
En segundo lugar, la inflamación local y sistémica inducida por la proteína de la espiga podría afectar a la señalización entre el cerebro y los ovarios (el eje hipotálamo-hipófisis-suprarrenal o eje HPA), provocando desequilibrios hormonales, la prolongación del reclutamiento folicular durante la parte inicial del ciclo y el alargamiento del ciclo.
Por otro lado, la vacunación durante la fase lútea puede suprimir el crecimiento del revestimiento endometrial y afectar a la estabilidad del endometrio, acortando así el ciclo.
En tercer lugar, la inflamación ovárica también puede estar causada por los efectos de las nanopartículas lipídicas (NPL) sobre las hormonas, una reacción autoinmune con anticuerpos antisintina en el endometrio o procesos inflamatorios desencadenados por la proteína de la espiga, ya sea de la vacuna o de la infección.
En cuarto lugar, las hemorragias anormales pueden deberse a una coagulación local anormal en el endometrio durante el periodo.
Un gran número de pruebas demostró que la proteína de la espiga puede desencadenar la cascada de coagulación mediante la inducción de la alteración endotelial, la inflamación de las células endoteliales, la liberación masiva de FvW activado, la sobreactivación de las plaquetas, la red fibrosa de las trampas extracelulares de neutrófilos (NET), así como el aumento del nivel de angiotensina II, la activación del receptor 4 tipo Toll, todo lo cual se suma para iniciar las cascadas de coagulación de la sangre.
Mientras tanto, la proteína de la espiga interrumpe los mecanismos de disolución del coágulo mediante la inducción de resistencia a la fibrinólisis, la unión competitiva al heparán sulfato, así como la formación de una sustancia similar al amiloide.
Basándose en las evidencias de las actividades de tipo dominó de la proteína espiga relacionadas con la coagulación sanguínea anormal, es probable que el papel potencial de la proteína espiga procedente de la vacuna SARS-CoV-2 o COVID-19 en la hemorragia anormal de las mujeres vacunadas contribuya al aumento de DCS y trastornos menstruales durante la pandemia de COVID, entre otras patologías inmunes y mediadas por hormonas desreguladas.
Impacto en la lactancia: Anticuerpos detectados en la leche y síntomas notificados
Un estudio prospectivo de cohortes incluyó a 50 mujeres lactantes que recibieron vacunas de ARNm con muestras de sangre y leche antes de su primera dosis de vacunación, inmediatamente antes de la segunda dosis y entre cuatro y diez semanas después de su segunda dosis.
Se midieron los anticuerpos anti-SARS-CoV-2 de dominio de unión al receptor (RBD) en cada muestra, y se recogieron muestras de sangre de un subconjunto de lactantes cuyas madres fueron vacunadas durante la lactancia.
Tras la vacunación, los niveles de IgG e IgM anti-SARS-CoV-2 aumentaron significativamente en el plasma materno y se produjo una transferencia significativa de anticuerpos IgA e IgG a la leche.
Los síntomas autodeclarados (fiebre, escalofríos, dolor de cabeza, dolor articular, dolores musculares o corporales y fatiga o cansancio) fueron notificados por un número significativamente mayor de participantes después de la 2ª dosis que después de la 1ª dosis.
Dos madres informaron de una producción de leche ligeramente menor en las primeras 24-72 horas después de las dosis de la vacuna.
El 12 por ciento de los lactantes presentaron al menos un síntoma tras la 1ª dosis materna de la vacuna, principalmente síntomas gastrointestinales y cambios en el sueño.
El estudio carecía de un control no vacunado y estos cambios en el comportamiento de los lactantes son frecuentes; futuros estudios deberían evaluar estos informes.
El estudio también recogió los síntomas tras la vacunación y observó que las personas que recibieron Moderna podían experimentar más efectos secundarios relacionados con la vacuna que las que recibieron Pfizer, lo que debería atribuirse de nuevo a la dosis más alta de Moderna.
Impacto de la inmunidad natural en la lactancia
Por último, un estudio de madres recientemente recuperadas de una infección por el SRAS-CoV-2 evaluó tanto los anticuerpos como las células T en la leche materna. Dado que solo una de cada cuatro mujeres decide vacunarse durante el embarazo, es importante evaluar la capacidad de la madre para conferir inmunidad pasiva a su hijo a través de la leche materna.
En este pequeño estudio de 30 mujeres lactantes, se evaluaron los parámetros de anticuerpos y células T en muestras de leche recogidas en 12 momentos a lo largo de un mes.
Se donó un segundo grupo de muestras cuatro meses después de un resultado positivo en la prueba del SRAS-CoV-2 para comprobar la durabilidad de los marcadores inmunitarios.
El estudio confirma que las mujeres recientemente infectadas por el SRAS-CoV-2 tienen anticuerpos en la leche que pueden neutralizar el complejo de espiga. La leche también está enriquecida con células T de memoria de la mucosa.
Este estudio puede ser el primero en demostrar que la leche materna de madres que se recuperaron de una infección por SRAS-CoV-2 contiene respuestas duraderas de anticuerpos IgA e IgG y que la leche materna puede proporcionar una protección pasiva al lactante a través de células T efectoras de memoria que pueden sembrar el tracto gastrointestinal del lactante.
Resumen de las principales observaciones
A partir de los datos disponibles recogidos de estudios clínicos, bases de datos de seguridad de vacunas o encuestas, se incluye un resumen de las observaciones clave:
1. Las preocupaciones sobre los impactos negativos de la vacunación COVID-19 en el ciclo menstrual fueron validadas por investigaciones revisadas por pares.
2. La duración del ciclo parece aumentar tras la vacunación tanto con ARNm como con adenovirus vectorizado, en particular para aquellas mujeres que recibieron ambas dosis dentro de un mismo ciclo (intervalo de 21-28 días), y aquellas que fueron vacunadas durante la fase folicular.
3. Los datos del VAERS sugieren un aumento del riesgo de irregularidades en la menstruación y el embarazo. Un estudio canadiense también observó mayores riesgos de acontecimientos adversos graves durante el embarazo asociados a la vacuna Moderna.
4. En Alemania y Suecia se notificaron fuertes descensos de las tasas de fertilidad total en 2022. Se informó de un descenso del 15 por ciento en la tasa de embarazo bioquímico y del 4,3 por ciento en la tasa de embarazo clínico, aunque los estudios de UMA no detectaron ningún cambio significativo.
5. La inflamación inducida por la proteína de la espiga, los trastornos inmunitarios y los mecanismos de acción mediados por hormonas, así como las cascadas de coagulación anormales y la sobreactivación, se correlacionaron con estos acontecimientos adversos clínicos.
6. Se detectaron anticuerpos inducidos por la vacuna COVID en la leche, así como síntomas entre las madres y los lactantes después de la vacunación.
7. El efecto se observó en todas las vacunas COVID-19 a base de proteínas, independientemente del tipo de vacuna. La vacuna de ARNm de dosis más alta (Moderna) se asocia con una mayor probabilidad de estos eventos que la vacuna de ARNm de dosis más baja (Pfizer).
Estos hallazgos sugieren claramente que es necesaria una vigilancia poscomercialización más rápida e intencionada para detectar los efectos de la vacunación en los acontecimientos relacionados con la menstruación, el embarazo y la lactancia.
Los CDC siguen recomendando la vacunación y las dosis de refuerzo para todas las personas mayores de 5 años a pesar de la falta de pruebas sobre una mayor reducción de las enfermedades graves por COVID-19 entre los menores de 40 años.
Para hacer frente a las dudas sobre las vacunas, los funcionarios de salud pública y los organismos reguladores deben demostrar que se tienen en cuenta las preocupaciones individuales y que los ensayos clínicos están diseñados para detectar efectos adversos poco frecuentes en personas jóvenes y por lo demás sanas antes de emitir recomendaciones generales.
Un despliegue gradual de los ensayos que dé prioridad a la inscripción de las personas de mayor riesgo y les haga un seguimiento de los criterios de valoración clínicamente importantes, como la hospitalización y la muerte, permitiría un rápido despliegue de las vacunas que salvan vidas, minimizando al mismo tiempo el daño a las personas con bajo riesgo de enfermedad grave.
Referencias:
1. Reproducción humana. The effect of Covid-19 mRNA vaccine on serum anti-Müllerian hormone levels.
2. Biomedicina reproductiva. The effect of SARS-CoV-2 mRNA vaccination on AMH concentrations in infertile women – PubMed (nih.gov)
3. Fertilidad y Esterilidad. Vacunación contra la enfermedad por coronavirus 2019 y resultados del tratamiento de la infertilidad – PubMed (nih.gov)
4. Obstetricia y Ginecología. Resultados de la fecundación in vitro y del embarazo precoz tras la vacunación contra la enfermedad por coronavirus 2019 (COVID-19) – PubMed (nih.gov)
5. Reproducción humana. Ovarian follicular function is not altered by SARS-CoV-2 infection or BNT162b2 mRNA COVID-19 vaccination – PubMed (nih.gov)
6. Obstetricia y Ginecología. Asociación entre la duración del ciclo menstrual y la vacunación contra la enfermedad por coronavirus 2019 (COVID-19): Una cohorte estadounidense – PubMed (nih.gov)/
7. Revista internacional de ginecología y obstetricia. El efecto de la vacuna BNT162b2 SARS-CoV-2 mRNA sobre los síntomas del ciclo menstrual en mujeres sanas – PMC (nih.gov)
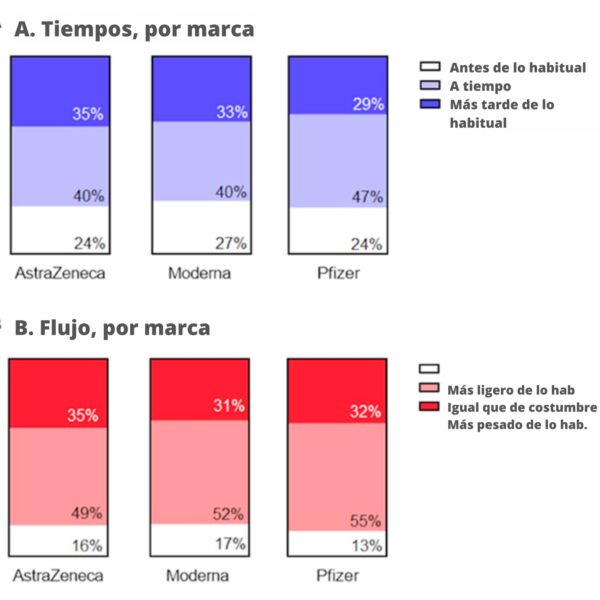
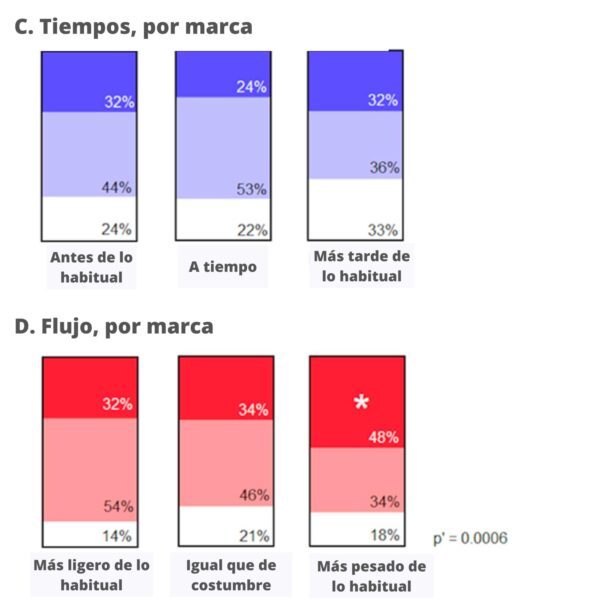
8. Fronteras en Salud Reproductiva. Efecto de la vacunación COVID-19 sobre el calendario y el flujo de los periodos menstruales en dos cohortes (frontiersin.org)
10. Fronteras de la Medicina. Análisis de la lesión ovárica asociada a la enfermedad por COVID-19 en mujeres en edad reproductiva en Wuhan, China: Un estudio observacional – PubMed (nih.gov)
11. Revista Americana de Obstetricia y Ginecología. Infección por SARS-CoV-2 y cambios posteriores en el ciclo menstrual entre las participantes en el estudio CoVHORT de Arizona (nih.gov)
13. Reproducción humana molecular. Influencia potencial de COVID-19/ACE2 en el sistema reproductor femenino – PubMed (nih.gov)
14. Revista Americana de Medicina Tropical e Higiene. Infección por COVID-19 en el tracto reproductor humano de hombres y mujeres no embarazadas – PubMed (nih.gov)
15, Medicina digital del Nature Publishing Group (NPJ). Vacunación con Covid-19 y duración del ciclo menstrual en el estudio Apple Women’s Health Study – PubMed (nih.gov)
16. Revista Americana de Obstetricia y Ginecología. A prospective study of the association between SARS-CoV-2 infection and COVID-19 vaccination with changes in usual menstrual cycle characteristics – American Journal of Obstetrics & Gynecology (ajog.org)
17. Lancet Infectious Disease. Safety of COVID-19 vaccines in pregnancy: a Canadian NationalVaccine Safety (CANVAS) network cohort study – PubMed (nih.gov)
18. Fronteras de la Inmunología.https://pubmed.ncbi.nlm.nih.gov/34804068/ COVID-19 mRNA Vaccination in Lactation: Evaluación de acontecimientos adversos y anticuerpos relacionados con la vacuna en díadas madre-lactante – PubMed (nih.gov)
19. Fronteras de la inmunología. Respuestas duraderas de anticuerpos y células T efectoras de memoria en la leche materna de mujeres con SARS-CoV-2 – PubMed (nih.gov)
21. Departamento de Salud y Servicios Humanos de los Estados Unidos (DHHS), Servicio de Salud Pública (PHS), Administración de Alimentos y Medicamentos (FDA)/Centros para el Control de Enfermedades (CDC). Vaccine adverse event reporting system (VAERS) 1990-last Friday, CDC WONDER Online Database. Términos de la búsqueda: Síntomas: Sangrado menstrual abundante, menstruación irregular, trastorno menstrual, sangrado intermenstrual, retraso menstrual, amenorrea, polimenorrea, oligomenorrea, menometrorragia, menorragia, metrorragia, gestión del ciclo menstrual. Vacuna: COVID-19 (consultado el 15 de abril de 2022). https://wonder.cdc.gov/controller/datarequest/D8.
Las opiniones expresadas en este artículo son las del autor y no reflejan necesariamente los puntos de vista de The Epoch Times.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.