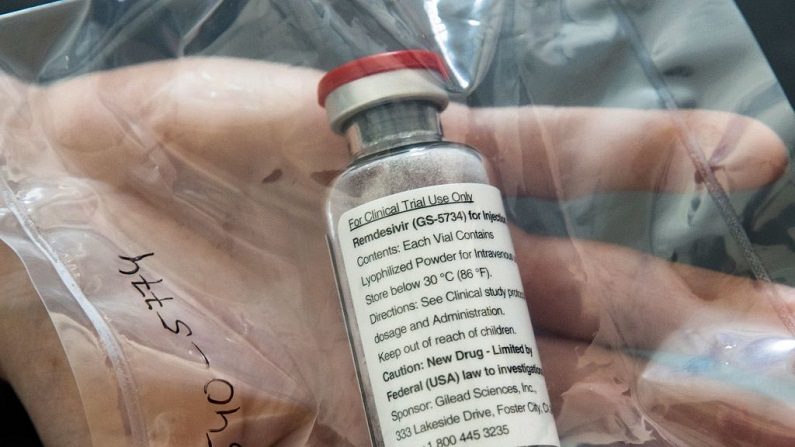
La Administración de Alimentos y Medicamentos de EE.UU. (FDA) aprobó el 14 de julio el uso de Veklury, también conocido como remdesivir, para tratar COVID-19 en personas con insuficiencia renal grave, incluida la diálisis, a pesar de los datos que demuestran que el fármaco aumenta el riesgo de insuficiencia renal.
El remdesivir es un medicamento antivírico que actúa sobre el ARN de los virus para impedir su replicación. La FDA autorizó por primera vez el remdesivir para uso de emergencia en mayo de 2020 para tratar a personas con COVID-19 grave. Desde entonces, se ha aprobado para adultos y niños de hasta 28 días de edad que pesen al menos 6.6 libras.
Remdesivir es el primer y único tratamiento antiviral contra COVID-19 aprobado por la FDA para personas con enfermedad renal.
La aprobación en EE.UU. sigue a la decisión de la Comisión Europea del 26 de junio de ampliar el uso aprobado de Veklury para tratar COVID-19 en personas con insuficiencia renal grave. La información actualizada sobre la prescripción de remdesivir no exige ajustar la dosis para los pacientes con insuficiencia renal y elimina el requisito de que los pacientes se sometan a una prueba de tasa de filtración glomerular estimada, la forma más fiable de medir el funcionamiento de los riñones antes de tomar el medicamento.
«La aprobación por parte de la FDA de Veklury para el tratamiento de pacientes con insuficiencia renal refleja la urgencia de poner este medicamento a disposición de estos pacientes, y subraya el perfil de seguridad establecido para Veklury», declaró en un comunicado de prensa Anu Osinusi, vicepresidente de Investigación Clínica para Hepatitis, Respiratorio y Virus Emergentes de Gilead Sciences.
Según la empresa, la FDA basó su aprobación del remdesivir para su uso en pacientes con insuficiencia renal grave en los resultados de un estudio de fase 1 y un ensayo de fase 3 aleatorizado, doble ciego, controlado con placebo, de grupos paralelos y multicéntrico que evaluó cómo interacciona el fármaco con el organismo y su perfil de seguridad. Sin embargo, el estudio de fase 3 finalizó prematuramente debido a «problemas de viabilidad» y a que «no tenía la potencia suficiente para evaluar la eficacia debido a que el número de participantes fue inferior al previsto».
La empresa afirmó que sus datos no revelaron ninguna nueva señal de seguridad «asociada al aumento de los niveles de metabolitos en pacientes con función renal gravemente reducida.» Sin embargo, los datos del estudio de fase 3 muestran que los acontecimientos adversos graves fueron significativamente mayores en quienes recibieron remdesivir que en quienes recibieron el placebo. Las personas que tomaron remdesivir fueron más propensas a sufrir lesión renal aguda (LRA), sepsis, neumonía COVID-19, muerte súbita y problemas cardiacos.
«Para empezar, el remdesivir nunca debería haberse aprobado», declaró a The Epoch Times el Dr. Paul Marik, médico de cuidados intensivos y autor de más de 500 artículos en revistas especializadas. «Gilead tuvo que manipular los datos para obtener la aprobación. Los propios datos de la Organización Mundial de la Salud (OMS) muestran que multiplica por veinte el riesgo de insuficiencia renal, así que por qué lo aprobarían para alguien con disfunción renal es obsceno».
La OMS publicó un boletín en 2020 en el que recomendaba no utilizar remdesivir para tratar la COVID-19. Las recomendaciones de la OMS se basaban en una revisión de las pruebas publicadas en el British Medical Journal, incluidos los datos de cuatro ensayos internacionales que abarcaron a más de 7000 pacientes hospitalizados por COVID-19. La OMS no encontró pruebas de que el tratamiento ayudara a los pacientes hospitalizados a recuperarse o mejorara sus resultados.
El Dr. Marik dijo que los Institutos Nacionales de Salud y Gilead «cocinaron el primer estudio» que formó la base inicial de la autorización de la FDA en octubre de 2020 porque remdesivir era «tan tóxico».
«Cometieron fraude científico en un solo estudio clínico que proporcionó datos a la FDA, cambiando el punto final a mitad del estudio para tratar de demostrar que el medicamento tenía algún beneficio», agregó. «La FDA es un apoderado de Big Pharma. No tiene ningún interés en la salud pública».
Numerosos estudios relacionan el Remdesivir con graves problemas renales.
En un estudio publicado en diciembre de 2020 en Clinical Pharmacology and Therapeutics, los investigadores detectaron una señal de seguridad para remdesivir y nefrotoxicidad —un rápido deterioro de la función renal debido a daños por un fármaco, sustancia química o toxina.
Utilizando una combinación de los términos «insuficiencia renal aguda» y «remdesivir» en el sistema VigiBase de la OMS —que recoge notificaciones espontáneas de sospechas de reacciones adversas a medicamentos de más de 130 países— se observó una «señal de desproporcionalidad estadísticamente significativa» con 138 casos en lugar de los nueve esperados. Además, la odds ratio de insuficiencia renal aguda con remdesivir fue veinte veces superior a la de los fármacos comparativos.
Un estudio publicado en marzo de 2022 en Frontiers identificó una asociación significativa entre la IRA y remdesivir en pacientes COVID-19 utilizando datos del Sistema de Notificación de Efectos Adversos de Vacunas, especialmente en pacientes varones de edad avanzada y mayores de 65 años.
Un análisis de farmacovigilancia de mayo de 2021 descubrió que «en comparación con el uso de cloroquina, hidroxicloroquina, dexametasona, sarilumab o tocilizumab, el uso de remdesivir se asoció con un aumento de la notificación de trastornos renales».
Como parte del mismo análisis, los investigadores evaluaron 5532 informes relacionados con pacientes de COVID-19 de la base de datos de la OMS, e identificaron 434 casos relacionados con trastornos renales, entre ellos 327 notificados con remdesivir.
El tratamiento con remdesivir se interrumpió poco después de la aparición del trastorno renal, con una duración media del tratamiento de tres días. En 316 casos, no se sospechó de ningún otro fármaco en la aparición de los trastornos renales. Las reacciones fueron graves en 301 casos (92%), y 15 pacientes fallecieron. La lesión renal aguda se presentó en 295 casos, con necrosis tubular en ocho.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.