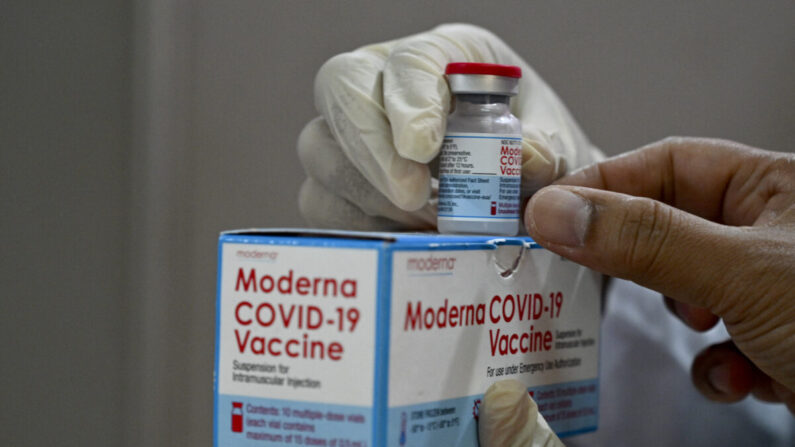
La decisión de la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) de acortar el tiempo de intervalo para la vacuna contra el COVID-19 de Moderna a cinco meses se basó en pruebas científicas que incluían la información de seguridad de las vacunas de refuerzo de Pfizer administradas en Israel, escribió el regulador sanitario en su carta de autorización a Moderna.
El regulador sanitario anunció el viernes que había modificado su autorización de uso de emergencia para la vacuna COVID-19 de Moderna, acortando a cinco meses el intervalo de seis meses entre la finalización de la serie de dos dosis y el refuerzo. Este cambio coincide con la revisión anterior de la FDA para la vacuna contra el COVID-19 de Pfizer.
La FDA argumenta que el cambio es necesario debido a la «variante ómicron altamente contagiosa, que se propaga más rápidamente» que el virus original y otras variantes hasta ahora.
La FDA afirma haber revisado varias publicaciones que no fueron citadas en la carta junto con los datos de los 4.1 millones de ciudadanos de Israel que han recibido el refuerzo de la vacuna de Pfizer.
«Para la autorización del 7 de enero de 2022, que revisa el intervalo de dosificación autorizado de la dosis de refuerzo homóloga a por lo menos 5 meses después de la finalización de la serie primaria, la FDA revisó: prepublicaciones; publicaciones aceptadas; publicaciones publicadas; y evidencia del mundo real sobre la seguridad de las dosis de refuerzo proporcionada por el Ministerio de Salud de Israel, que incluye datos de aproximadamente 4.1 millón de terceras dosis (de refuerzo) de la vacuna COVID-19 de Pfizer-BioNTech administradas a personas de 16 años o más al menos 5 meses después de la serie primaria, y que no plantearon nuevos problemas de seguridad asociados a la dosis de refuerzo», escribió la FDA (pdf).
El regulador sanitario federal reconoció que la composición general de las dos vacunas de ARN mensajero difería, pero como «ambas son vacunas de ARNm» «son relativamente similares».
«Reconociendo las diferencias, es razonable inferir que los datos de seguridad sobre el intervalo de [cinco] meses para las dosis de refuerzo obtenidos en la población de Israel pueden aplicarse a la vacuna contra COVID-19 de Moderna», dijo la FDA.
La revisión sobre la dosis de refuerzo de Moderna suscitó las críticas del Dr. Vinay Prasad, hematólogo-oncólogo y profesor asociado de epidemiología en la Universidad de California-San Francisco, quien argumentó que la decisión de la FDA no se basaba en pruebas científicas y que «NO ES RAZONABLE tomar una determinación sobre Moderna a partir de los datos de Pfizer».
«La FDA ya ni siquiera lo intenta; La decisión se basa en los datos de PFIZER no en los de MODERNA, lo cual reconocen en la carta de hoy», dijo Prasad en un tuit. «Literalmente no hay [sic] NINGUNA EVIDENCIA para el refuerzo de MODERNA en el mes 5».
La FDA ya ni siquiera lo intenta;
La decisión se basa en los datos de PFIZER y no en los de MODERNA, lo que reconocen en la carta de hoyLiteralmente, no hay ninguna evidencia para el refuerzo de MODERNA en el mes 5 ??
Gruber y Krause renuncian y la FDA está desquiciada https://t.co/TDOIzQHsWr pic.twitter.com/W6HxUb2Pum
— Vinay Prasad, MD MPH ?️? (@VPrasadMDMPH) 7 de enero de 2022
También comparó las dosis de las dos vacunas de ARNm, diciendo que «la dosis de Moderna es de 100, 100 y 50 de refuerzo; la de Pfizer es de 30, 30, 30», añadiendo que «Moderna tiene muchas más [posibilidades de] miocarditis».
Según los Centros de Enfermedades y Prevención (CDC, por sus siglas en inglés), «desde abril de 2021, se ha informado de un aumento de los casos de miocarditis [inflamación del corazón] y pericarditis [inflamación del tejido que rodea el corazón] en Estados Unidos después de la vacunación con [vacunas de] ARNm contra COVID-19 (Pfizer-BioNTech y Moderna), especialmente en adolescentes y adultos jóvenes».
El aumento de la miocarditis y la pericarditis después de recibir una vacuna de ARNm hizo que la FDA actualizara sus hojas informativas para pacientes y proveedores en junio de 2021, advirtiendo de un mayor riesgo de efectos secundarios graves después de la vacunación.
Cuando se le preguntó por qué la FDA basó su decisión en los datos de seguridad de Pfizer en lugar de los datos de refuerzo de la vacuna de Moderna, un portavoz de la FDA, en un correo electrónico a The Epoch Times, proporcionó un enlace a la carta de autorización y dijo que un «memorando que resume nuestra decisión debería publicarse muy pronto».
The Epoch Times se ha puesto en contacto con Moderna para solicitar comentarios.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.