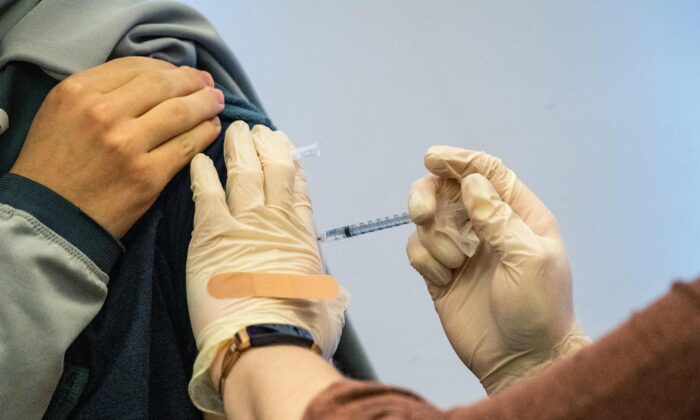
Científicos de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) afirmaron el 13 de junio que la vacuna contra COVID-19 de Pfizer funcionó bien en niños pequeños, pese a que más participantes vacunados que los no vacunados en el ensayo clínico de Pfizer experimentaron enfermedades graves.
Los datos del ensayo demuestran que es eficaz «en la prevención de COVID-19 en el grupo de edad comprendido entre los 6 meses y los 4 años», señalaron los científicos de la FDA en un documento escrito (pdf) presentado ante su panel asesor de vacunas.
Además, los datos indican que «probablemente tendrán un efecto beneficioso» sobre la hospitalización y la muerte, sostuvieron los científicos.
La FDA dijo que concederá la solicitud de autorización de uso de emergencia de Pfizer y BioNTech, las compañías que fabricaron la vacuna conjuntamente.
La vacuna de Pfizer es la única disponible para los niños en Estados Unidos. La empresa pretende ampliar esa disponibilidad a niños desde los 6 meses.
La solicitud se modificó este año, pasando de una serie primaria de 2 dosis a una serie primaria de 3 dosis porque la serie de 2 dosis no desencadenó una respuesta inmunitaria adecuada en algunos de los niños.
El aumento de la dosis cumplió el objetivo principal, que era un determinado nivel de anticuerpos neutralizantes aceptado como marcador de protección contra el virus del PCCh (Partido Comunista Chino). También conocido como SARS-CoV-2, el virus causa el COVID-19.
La vacuna de Moderna, también en fase de autorización de emergencia para los niños, no dio buenos resultados contra la infección, pero Pfizer sí, con una eficacia estimada del 80%.
Sin embargo, en el ensayo de Pfizer hubo más niños vacunados que sufrieron estados graves de COVID-19 en comparación con los niños no vacunados.
«Entre todos los casos de COVID-19 acumulados desde la dosis 1 hasta el corte de datos del 29 de abril de 2022, 1 receptor de placebo de 6 a 23 meses de edad y 7 participantes de 2 a 4 años de edad (6 receptores de BNT162b2 y 1 receptor de placebo) cumplieron los criterios especificados por el protocolo para COVID-19 grave durante el seguimiento ciego y abierto», dijeron los científicos de la FDA en el nuevo documento.
Además, el único niño que requirió hospitalización había recibido la vacuna.
Los reguladores trataron de restar importancia a los casos, diciendo que todos menos uno cumplían los criterios de caso grave «en base a los hallazgos de signos vitales que no eran clínicamente significativos en opinión del investigador y de la FDA». Los científicos de la agencia dijeron entonces que la vacuna «probablemente tendrá un efecto beneficioso» sobre la hospitalización y la muerte. También dijeron que los datos de seguridad no planteaban nuevas preocupaciones.
Los datos de eficacia se basaron en solo 363 niños participantes. Los datos de seguridad procedían de unos 3000 voluntarios.
El documento se presentó dos días antes de que la FDA y Pfizer hicieran presentaciones ante el Comité Asesor de Vacunas y Productos Biológicos Relacionados, un panel que asesora a la FDA sobre las vacunas.
«No puedo creer que este comité recomiende siquiera la autorización con este tipo de datos», dijo a The Epoch Times Kim Witczak, quien dirige el grupo de defensa de la seguridad de los medicamentos Woody Matters y forma parte de otro panel consultivo de la FDA, tras revisar los documentos que se han presentado al panel.

Witczak es una de las personas que no está de acuerdo con que la FDA haya permitido a los fabricantes de medicamentos utilizar la inmunidad, o el nivel de anticuerpos, como principal criterio de valoración de los ensayos, en lugar de la eficacia clínica. El especialista cree que la emergencia de COVID-19 ha terminado, lo que significa que la FDA no puede conceder una autorización de uso de emergencia. También señaló que Pfizer volvió a desenmascarar a los participantes en el ensayo, o notificar al grupo de placebo que podía recibir una vacuna, lo que socava los resultados del estudio.
Los científicos de Pfizer afirmaron en un informe separado (pdf) que los datos del ensayo muestran que la vacuna de la empresa «ofrece una protección medible contra la COVID-19 sintomática» en niños pequeños.
Los científicos de la FDA dijeron que había incertidumbres en relación con las vacunas, incluida la durabilidad de la protección que ofrecen. También señalaron que «probablemente» se necesitaría una tercera inyección de Moderna y una cuarta de Pfizer para aumentar la eficacia después de que ésta disminuya, lo que ha ocurrido en grupos de mayor edad. El análisis de la agencia indicó que el riesgo de inflamación del corazón después de la vacunación, una condición que no se detectó en los ensayos originales, «es desconocido» para los niños pequeños.
El panel asesor de la FDA puede aconsejar o no a la FDA que autorice las vacunas de Pfizer y Moderna. La FDA a su vez puede ignorar las recomendaciones.
Si la FDA autoriza una o ambas vacunas, los Centros para el Control y la Prevención de Enfermedades decidirán si recomiendan las vacunas para los niños.
La Casa Blanca dijo a su vez que las vacunas podrían administrarse a los niños pequeños ya en la semana del 20 de junio.
Si se autoriza, la vacuna de Pfizer se administraría a los niños pequeños en tres dosis en un plazo de apenas 11 semanas. La dosis, de 3 microgramos cada una, es una décima parte de la que se administra a los grupos de mayor edad. La serie de dos dosis de Moderna se administraría en un mes. El nivel de dosis, 25 microgramos, es una cuarta parte del que se administra a poblaciones de mayor edad.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.