El Tribunal Supremo ha programado la vista oral de un recurso contra la normativa que regula el uso de la píldora abortiva mifepristona.
La esperada vista tendrá lugar el 26 de marzo, según anunció el tribunal el 29 de enero. El tribunal concedió la petición de certiorari, o revisión, en el caso, el 13 de diciembre de 2023.
La Corte Suprema considerará si la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) siguió la ley federal cuando relajó las restricciones en 2016 y 2021 sobre la píldora.
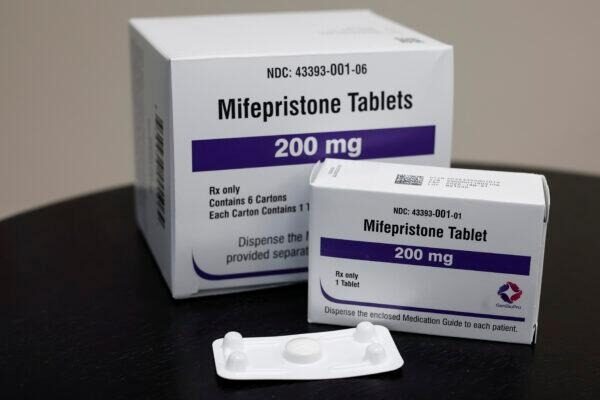
Un aborto farmacológico implica generalmente el uso de mifepristona, que bloquea la progesterona, una hormona, y misoprostol, que induce contracciones. El misoprostol, que está ampliamente disponible porque tiene muchos usos médicos, no es objeto del litigio actual.
Los defensores de la mifepristona afirman que el sistema actual de suministro del fármaco es seguro, mientras que sus detractores afirman que pone en peligro a las mujeres al ignorar los protocolos de seguridad vigentes en 2016 y 2021.
Al gobierno de Biden y a los grupos proabortistas les preocupa que la eventual decisión de la Corte Suprema en el caso pueda afectar la disponibilidad del medicamento.
Lo que está en juego en este caso, ampliamente litigado, es la decisión de la FDA en 2016 de flexibilizar las normas de prescripción de la mifepristona y, en 2021, de permitir que las recetas se envíen por correo sin que la paciente acuda primero a un médico en persona.
En realidad, se trata de dos casos consolidados: FDA contra Alliance for Hippocratic Medicine (AHM) y Danco Laboratories LLC contra AHM.
Danco Laboratories fabrica mifepristona, también conocida como mifeprex y RU-486.
El caso es el más importante de la Corte Suprema relacionado con el aborto desde su decisión de junio de 2022 en Dobbs v. Jackson Women’s Health Organization, que determinó que no existía el derecho al aborto en la Constitución de EE.UU.
Ese fallo anuló el caso Roe contra Wade (1973) y devolvió la regulación del aborto a los estados.
En una repetición virtual de 2022 y el caso Dobbs, se espera la decisión para junio, momento en el que podría convertirse en una cuestión política en las elecciones de noviembre. Los comentaristas afirman que si el tribunal vuelve a imponer las antiguas restricciones sobre la mifepristona, es probable que los votantes culpen a los republicanos y que los demócratas salgan beneficiados políticamente.
El juez Matthew Kacsmaryk de la corte de distrito de Estados Unidos para el Distrito Norte de Texas, un designado del presidente Donald Trump, dictaminó en abril de 2023 que la FDA se equivocó al aprobar la mifepristona para uso público en 2000 y que la agencia había arrastrado deliberadamente la revisión judicial del medicamento durante años.
El juez también determinó que la FDA había levantado indebidamente las restricciones relacionadas con el acceso al fármaco.
El juez Kacsmaryk dictó una medida cautelar de ámbito nacional que suspendía retroactivamente la aprobación de la FDA. Escribió que la FDA no había evaluado adecuadamente los riesgos que planteaba el fármaco antes de aprobarlo, cediendo ante la presión política para sacarlo al mercado.
En este caso, la FDA «consintió en sus preocupaciones legítimas de seguridad -en violación de su deber estatutario- basándose en un razonamiento claramente infundado y en estudios que no apoyaban sus conclusiones», escribió.
«También hay pruebas que indican que la FDA se enfrentó a una importante presión política para renunciar a sus precauciones de seguridad propuestas para avanzar mejor en el objetivo político de aumentar el ‘acceso’ al aborto químico».
El hecho de que la FDA no impusiera restricciones al uso del fármaco «provocó muchas muertes y muchas más reacciones adversas graves o potencialmente mortales», escribió.
La normativa ha cambiado a lo largo de los años.
En 2016, la FDA modificó la etiqueta del medicamento, ampliando el corte para su uso de 49 días de gestación a 70 días. Al mismo tiempo, la agencia permitió que el medicamento se prescribiera con una sola visita en persona y detuvo el requisito de que los prescriptores informaran los eventos adversos no mortales relacionados con el medicamento.
Recibirlo por correo
En 2019, la FDA aprobó una versión genérica del medicamento. En 2021, la agencia permitió a las pacientes recibir el medicamento por correo en lugar de tener que recogerlo en persona de un proveedor de atención médica especialmente certificado.
El Departamento de Justicia de EE.UU. (DOJ) apeló la decisión del juez Kacsmaryk, pero la Corte de Apelaciones de EE.UU. para el 5º Circuito, de tendencia conservadora, se negó a bloquear la mayor parte de la orden.
El 5º Circuito sostuvo que las acciones de la FDA en 2016 y 2021 eran probablemente ilegales-un hallazgo que la FDA y Danco pidieron a la Corte Suprema que revisara.
En agosto de 2023, el 5º Circuito confirmó las restricciones impuestas por el juez de distrito a la píldora abortiva, sosteniendo que la FDA no tuvo debidamente en cuenta las cuestiones de seguridad pública al aprobarla.
Gran parte de la opinión de la corte del circuito se centra en la cuestión legal de la legitimación, cuya ausencia suele condenar una demanda.
El 5º Circuito observó que la AHM y los demás demandantes alegaron que tenían «capacidad asociativa» porque las diversas organizaciones implicadas en la demanda tienen miembros que «probablemente sufran perjuicios como consecuencia de las acciones de la FDA».
La corte encontró que los demandantes «hicieron una ‘clara demostración’ de que sus miembros se enfrentan a un perjuicio con suficiente probabilidad como para apoyar la adopción de una medida cautelar.»
El DOJ apeló a la Corte Suprema, que en abril de 2023 bloqueó la medida cautelar sobre la aprobación original del fármaco en 2000, permitiendo que la mifepristona siguiera en el mercado. Los jueces conservadores Clarence Thomas y Samuel Alito votaron en contra de levantar la medida cautelar.
En septiembre de 2023, la fiscal general de EE.UU., Elizabeth Prelogar, instó a la Corte Suprema a actuar, diciendo que el fallo del 5º Circuito era la primera vez que una corte había cuestionado el «juicio experto» de la FDA en la aprobación de medicamentos.
Si la sentencia se mantiene intacta, «impondría graves perjuicios al gobierno, a los patrocinadores de la mifepristona, a las mujeres que solicitan abortos farmacológicos y al público», afirmó entonces.
Prelogar presentó una nueva demanda el 23 de enero, en la que argumentaba que la medida cautelar de la corte de distrito causaría «un trastorno a nivel nacional que amenazaría con causar profundos daños al gobierno, al sistema sanitario, a los pacientes y al público».
Además, la acción de la FDA en 2016 fue respaldada por «una revisión exhaustiva de un registro que incluye docenas de estudios científicos y décadas de uso seguro de la mifepristona por millones de mujeres en los Estados Unidos y en todo el mundo», escribió.
«La pérdida de acceso a la mifepristona sería perjudicial para las mujeres y los proveedores de atención médica en todo el país».
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.





