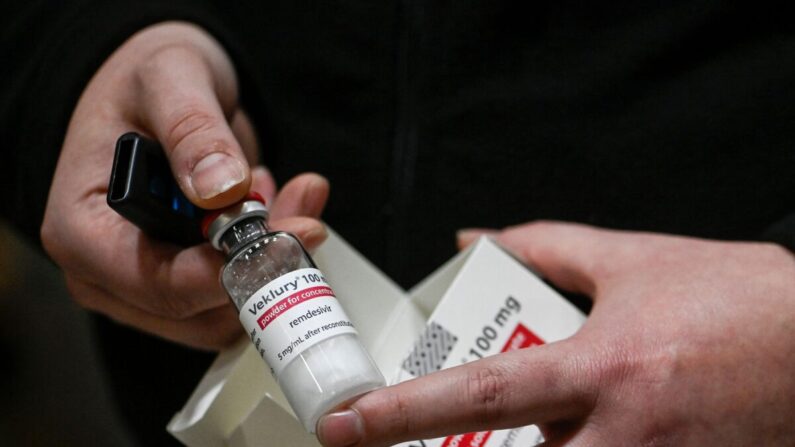
La empresa que fabrica el remdesivir, medicamento utilizado en Estados Unidos para tratar COVID-19, fue objeto de una demanda colectiva por presuntas prácticas engañosas en la promoción del fármaco sin revelar sus posibles efectos secundarios.
Dos residentes de California, uno de las cuales es familiar de una persona que falleció tras recibir remdesivir, presentaron la demanda contra Gilead Sciences en el condado de Shasta el 26 de septiembre.
Deborah Fust, cónyuge sobreviviente de Michael Fust, y Edward Pimentel, que afirma haber sufrido lesiones tras recibir remdesivir, acusaron a Gilead, con sede en California, de no mencionar los efectos secundarios documentados en su promoción de remdesivir.
«Este es un medicamento terrible. La organización sin ánimo de lucro cuenta con miles de miembros que tienen los historiales hospitalarios, y se puede ver que hay una gran diferencia en los niveles de creatinina y los niveles sanguíneos, las lecturas renales después de recibir el remdesivir», declaró a The Epoch Times Bradford Geyer, abogado del Former Feds Group que representa a los demandantes.
La fundación sin ánimo de lucro FormerFedsGroup Freedom Foundation recopiló algunos de los casos en su sitio web.
La demanda afirma que los comunicados de prensa y las declaraciones de Gilead a los consumidores y a los investigadores muestran «un patrón de minimización u omisión total de los peligros clínicos experimentados por los pacientes por el uso de remdesivir, en lugar, enfatizando sus supuestos beneficios, seguridad y eficacia».
Por ejemplo, en un sitio web del medicamento, también conocido como Veklury, no se mencionan los problemas renales. Un folleto (pdf) que se entrega a los pacientes tampoco menciona estos problemas.
«La publicidad del demandado de que el remdesivir es un tratamiento seguro y eficaz contra COVID-19 es falsa y engañosa para un consumidor razonable, incluidos los demandantes, porque el demandado sabía o debería haber sabido, basándose en estudios y datos anteriores sobre el remdesivir, que no era seguro y que planteaba un alto riesgo de efectos adversos graves y de muerte para los demandantes y el grupo», afirma la demanda.
La publicidad «tergiversaba y/u omitía el verdadero contenido y la naturaleza del medicamento», dice también la demanda.
Gilead no respondió a la solicitud de comentarios.
Los demandantes solicitan la condición de colectivo, lo que permitiría a dos grupos de personas unirse a la demanda. Se trata de personas que recibieron remdesivir mientras estaban hospitalizadas con COVID-19 y sufrieron lesiones graves a consecuencia de ello, y personas cuyos seres queridos fallecieron tras recibir remdesivir después de estar hospitalizados con COVID-19.
Autorización anticipada de la FDA
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) concedió una autorización de emergencia a Gilead para el remdesivir en mayo de 2020, basándose principalmente en los resultados de un ensayo patrocinado por el gobierno en el que los investigadores cambiaron el criterio de valoración a mitad de camino. Los críticos afirmaron que el cambio se hizo para obtener resultados positivos. El ensayo descubrió que remdesivir aceleraba el tiempo de recuperación de COVID-19.
La agencia tomó la decisión sin consultar a su comité asesor sobre medicamentos antimicrobianos.
La FDA aprobó el remdesivir en octubre de 2020 y amplió su uso permitido a pacientes ambulatorios y niños.
Poco después, un gran ensayo dirigido por la Organización Mundial de la Salud encontró que el remdesivir no aceleraba el tiempo de recuperación ni reducía la mortalidad. El grupo desaconsejó el uso de remdesivir en pacientes hospitalizados, lo que iba en contra de la recomendación de Estados Unidos.
Los estudios con animales encontraron indicios de que el remdesivir dañaba el riñón. El ensayo estadounidense halló lesiones renales entre los receptores de remdesivir, incluso en tres pacientes que se vieron obligados a dejar de tomar el fármaco.
Otros estudios, así como datos posteriores a la aprobación, también suscitaron preocupaciones sobre la seguridad y la eficacia.
Por ejemplo, los investigadores que revisaron los informes enviados a VigiBase, una base de datos de la Organización Mundial de la Salud, descubrieron que los informes de lesiones renales tras recibir remdesivir eran muy superiores a los informes de lesiones renales tras otros tratamientos contra COVID-19.
Antes de recibir remdesivir, la FDA indica a los pacientes estadounidenses (pdf) que revelen todas sus afecciones médicas, incluidos los problemas renales.
Gilead, aunque promocionaba el remdesivir, necesitaba revelar el riesgo de lesiones renales, según la nueva demanda.
Al no hacerlo, la empresa supuestamente violó las leyes de California contra el uso de prácticas engañosas y la realización de declaraciones falsas o engañosas.
Gilead también hizo tergiversaciones negligentes, lo que resultó en un enriquecimiento injusto, dice la demanda.
Los demandantes buscan una orden que establezca una colectividad, una orden que impida a Gilead participar en «prácticas comerciales injustas, ilegales y engañosas y publicidad falsa», una orden que obligue a Gilead a corregir sus anuncios anteriores, una orden que ordene a Gilead retirar y destruir anuncios engañosos y materiales publicitarios engañosos, una orden que exija a Gilead devolver el dinero obtenido mediante las acciones supuestamente violatorias y una orden que obliga a Gilead a pagar restitución e intereses.
Los demandantes también quieren daños y perjuicios.
Después del fallo de Michigan
La nueva demanda surgió después de que una corte de Michigan dictaminara que el remdesivir no está protegido por la ley federal contra una acción legal presentada por un hombre que necesitó que le amputaran una pierna tras recibir el fármaco.
El hombre, Don Nowacki, también sufrió dos derrames cerebrales.
Se dijo que el remdesivir que recibió estaba contaminado con partículas de vidrio.
Gilead argumentó que no podía ser demandado debido a la inmunidad otorgada por la Ley de Preparación Pública y Emergencias, que fue activada por la administración Trump durante la pandemia de COVID-19.
El juez rechazó ese argumento y consideró que la ley no cubría al fabricante en la situación.
El Sr. Nowacki y sus abogados ahora están listos para ser habilitados, y el juicio se realizará más adelante.
«Una de las cosas que vamos a descubrir es exactamente qué sabían Gilead, la FDA y el hospital y cuándo», dijo Ven Johnson, uno de los abogados, a The Epoch Times. «¿Cómo estas partículas de vidrio, que podrían causar «accidentes cerebrovasculares y muerte en las personas, entraron en este medicamento? ¿Por qué estas personas no se acercan a nosotros para obtener los registros médicos de nuestros clientes para entender lo que sucedió?»
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.