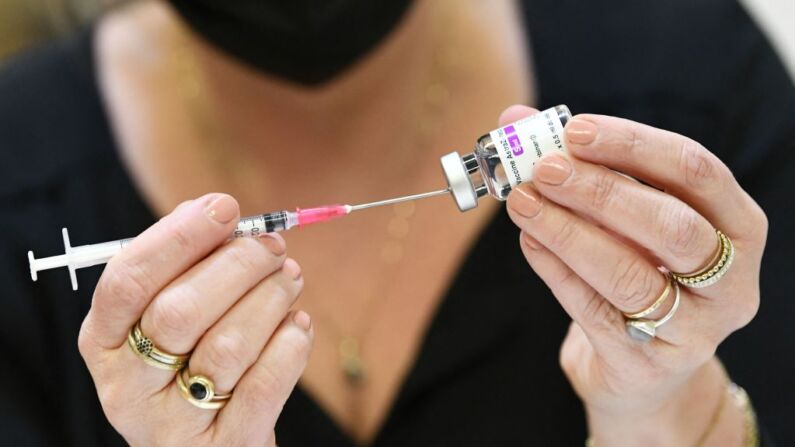
El regulador europeo de medicamentos dijo el viernes que no pudo confirmar si la vacuna COVID-19 de AstraZeneca tiene alguna incidencia en mayores riesgos de coágulos sanguíneos inusuales asociados a bajos niveles de plaquetas en sangre de mujeres y adultos jóvenes.
La Agencia Europea de Medicamentos (EMA) dijo en un comunicado que la Comisión Europea (CE) le solicitó que brindara una opinión científica tras los reportes iniciales de trombosis con síndrome de trombocitopenia (TTS) asociados a la vacuna contra COVID-19 de AstraZeneca, conocida como Vaxzevria.
«Las pruebas no permitieron a la EMA identificar los factores de riesgo particulares que hacen más probable el TTS», dijo el regulador de medicamentos.
“Aunque los reportes espontáneos (…) han indicado que el riesgo puede ser mayor en mujeres y adultos jóvenes, y menor tras la segunda dosis en comparación con la primera, las limitaciones de la forma en que se recopilan los datos hacen que no se pueda confirmar ninguna de estas diferencias».
Un comité que es responsable de elaborar los dictámenes de la EMA sobre todas las cuestiones relativas a los medicamentos de uso humano concluyó también un análisis adicional para determinar si el retraso de la segunda dosis de Vaxzevria tiene alguna influencia en el riesgo de TTS.
«No hay pruebas de que el retraso de la segunda dosis influya en el riesgo de TTS», dijo el comité.
La agencia europea de salud dijo que estaba reiterando que la segunda dosis puede continuar administrándose entre cuatro y 12 semanas después de la primera. También agregó que actualmente no se pueden dar recomendaciones definitivas sobre el uso de una vacuna diferente para una segunda dosis tras una primera dosis de AstraZeneca.
La EMA dijo que el estudio se basó en todos los datos disponibles relacionados con el TTS, incluidos los de una base de datos que se centra en la recopilación de sospechas de reacciones adversas a medicamentos autorizados o en estudio en ensayos clínicos en el Espacio Económico Europeo.
Vaxzevria de AstraZeneca es una vacuna de dos dosis desarrollada junto con la Universidad de Oxford.
El regulador de fármacos comenzó a investigar las condiciones adversas en abril luego de que se reportaran docenas de casos de coagulación sanguínea, incluidas muertes, en personas tras recibir la inyección.
Las reacciones adversas posiblemente relacionadas con la inyección llevaron a más de una docena de países a detener el uso de la vacuna contra COVID-19 de AstraZeneca a inicios de este año como medida de precaución, mientras los investigadores investigaban los casos reportados de coágulos de sangre entre las personas vacunadas.
Con información de Reuters.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.