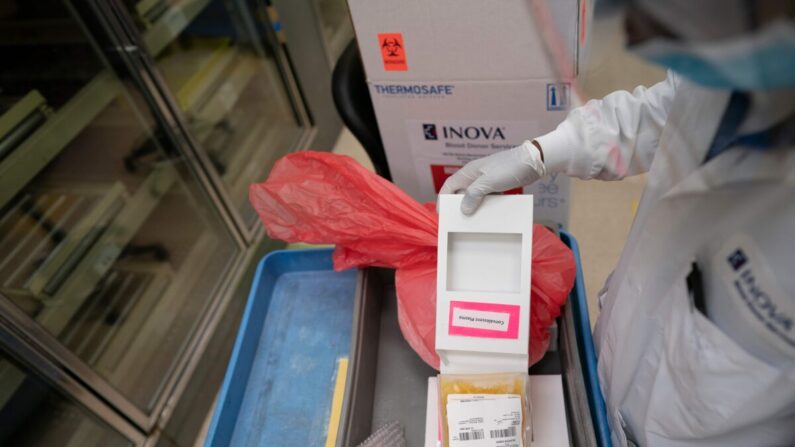
Análisis de noticias
Los datos sobre la eficacia del plasma de convaleciente para los pacientes hospitalizados por COVID-19 aún no son concluyentes, a pesar de que ha pasado más de un año desde que la autoridad federal emitió por primera vez una autorización de uso de emergencia (EUA) para la terapia y se han realizado muchos estudios.
Los resultados de un reciente ensayo controlado y aleatorizado sugieren que el plasma de convaleciente —el componente líquido de la sangre que contiene anticuerpos— procedente de personas que se recuperaron con éxito del COVID-19, no ayudó a los pacientes hospitalizados con la enfermedad y puede ser perjudicial.
Los investigadores, cuyo estudio se publicó en Nature Medicine el 9 de septiembre, afirmaron que el plasma de convaleciente no redujo el riesgo de intubación o muerte. Los investigadores sí señalaron que el variado contenido de anticuerpos del plasma de convaleciente podría haber modificado la respuesta al tratamiento.
«Se ha pensado que el plasma sanguíneo de los supervivientes del COVID-19 ayudaría a los enfermos graves del virus pero, por desgracia, no es así», dijo Donald Arnold, coautor del estudio y profesor de medicina de la Universidad McMaster.
«Advertimos contra el uso de plasma de convalecientes para tratar a los pacientes hospitalizados por COVID-19, a menos que estén en un ensayo clínico supervisado rigurosamente».
El estudio también reveló que los pacientes del grupo de plasma experimentaron más efectos adversos graves que los que recibieron el tratamiento estándar. La mayoría de los efectos secundarios fueron el empeoramiento de la hipoxemia, o el bajo nivel de oxígeno en sangre, y la insuficiencia respiratoria. Sin embargo, no hubo diferencias significativas en la tasa de efectos adversos mortales entre ambos grupos.
En el estudio participaron 938 pacientes de COVID-19 que recibieron plasma de convaleciente o la atención estándar en 72 hospitales de Estados Unidos, Canadá y Brasil entre el 14 de mayo de 2020 y el 29 de enero de 2021.
Los autores dijeron que los hallazgos fueron consistentes con un estudio aleatorio más grande, el ensayo RECOVERY que involucró a 11,558 pacientes hospitalizados con COVID-19 que «encontró que el riesgo de muerte después de la administración de plasma de título alto no fue diferente de la atención estándar».
En un estudio más reciente que aún no ha sido revisado por los expertos, los investigadores analizaron las variables que afectaban a la eficacia del plasma de convaleciente en 23 ensayos controlados aleatorios y descubrieron que, aunque había datos contradictorios sobre la eficacia clínica, el plasma de convaleciente reducía la mortalidad en muchos de los estudios.
«Centrándonos solo en los resultados de los 23 ensayos controlados aleatorios disponibles, observamos que era más probable que éstos mostraran señales de eficacia, incluyendo reducciones en la mortalidad si el título neutralizante del plasma era ≥ 160 y el tiempo hasta la aleatorización era ≤ 9 días, lo que es coherente con la eficacia de la terapia pasiva de anticuerpos que requiere la dosificación con suficientes anticuerpos», escribieron los autores.
«El hecho de que la mayoría de los estudios revelaran señales de eficacia a pesar de la variabilidad del [plasma de convaleciente de COVID-19] y de su uso sugiere efectos terapéuticos sólidos que se hacen evidentes a pesar del ruido de los datos», añadieron los autores.
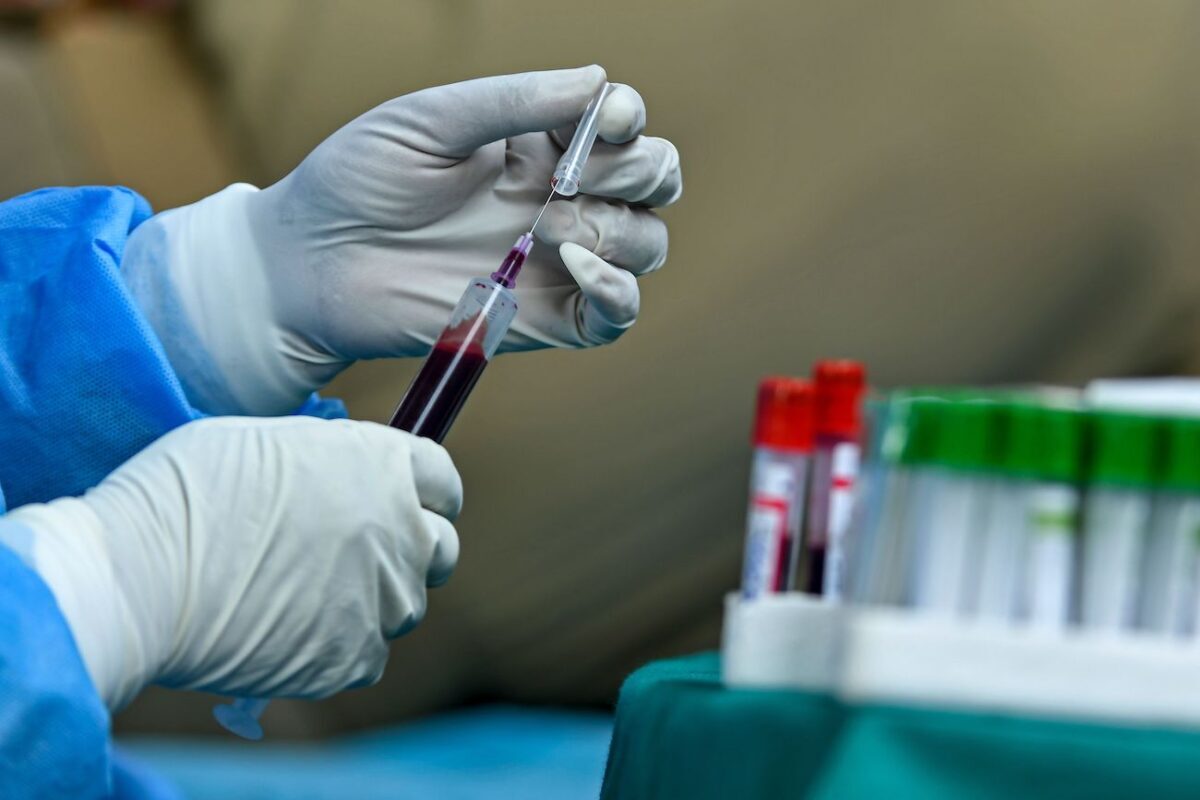
Uso de emergencia de plasma de convaleciente
Al principio de la pandemia, se pensó que el plasma de convaleciente podría disminuir la gravedad de la enfermedad o ayudar a los pacientes a recuperarse más rápidamente, como ocurrió en brotes virales anteriores.
Se cree que los anticuerpos del plasma pueden proporcionar inmunidad pasiva y beneficiar a los enfermos graves, ya que normalmente se tarda entre una y tres semanas en desarrollar una respuesta de anticuerpos tras la infección, según los Centros para el Control y la Prevención de Enfermedades (CDC).
El 23 de agosto de 2020, la FDA emitió la autorización de uso del plasma de convaleciente para el tratamiento de pacientes hospitalizados con COVID-19 confirmado o sospechoso. La autorización se basó en la evidencia disponible en ese momento, incluidos los datos del Programa de Acceso Expandido al Plasma de Convaleciente patrocinado por Mayo Clinic, que fue establecido por la FDA para aumentar el acceso al plasma en pacientes gravemente enfermos. El programa recibió 26 millones de dólares de la Autoridad de Investigación y Desarrollo Biomédico Avanzado.
En febrero de 2021, el regulador federal revisó el uso de emergencia para permitir únicamente la administración de plasma con altos niveles de anticuerpos, o plasma de convaleciente de título alto, de forma temprana a los pacientes de COVID-19 hospitalizados antes de que sufrieran una insuficiencia respiratoria o a los pacientes con inmunidad deteriorada.
El plasma de título alto se define como el que tiene niveles de anticuerpos neutralizantes de ≥250 según un ensayo de neutralización del Instituto Broad.
«Basándose en la totalidad de las pruebas científicas disponibles en este momento, los beneficios conocidos y potenciales del plasma de convaleciente de COVID-19 de título alto superan los riesgos conocidos y potenciales cuando se administra en una fase temprana de la enfermedad, y a los hospitalizados con la inmunidad humoral deteriorada», dijo la FDA en la hoja informativa entregada a los proveedores de atención médica.
La FDA dijo que los estudios han descubierto que el plasma con títulos bajos no era eficaz para tratar a los pacientes hospitalizados y que ya no lo autorizaría para su uso de emergencia. Los Institutos Nacionales de Salud (NIH, por sus siglas en inglés) también desaconsejan el uso de plasma con bajos niveles de anticuerpos.
Sin embargo, los NIH adoptaron una postura neutral en cuanto a la recomendación del plasma de convalecencia de título alto en pacientes externos con COVID-19 o que están hospitalizados con la inmunidad deteriorada, citando evidencia insuficiente. También aconseja a los médicos que no prescriban plasma de título alto en pacientes con ventilación mecánica, a menos que se trate de un ensayo clínico.
El Dr. Paul Marik, profesor de medicina y jefe de la División de Medicina Pulmonar y de Cuidados Críticos de la Facultad de Medicina del Este de Virginia, que ha estado tratando a pacientes con COVID-19 desde el comienzo de la pandemia, dice que el plasma de convaleciente solo es eficaz en pacientes que están «gravemente inmunodeprimidos».
«El suero de convaleciente no tiene ninguna importancia; la excepción son los que están gravemente inmunodeprimidos», dijo Marik a The Epoch Times por correo electrónico.
Marik es uno de los cofundadores de la Alianza de Cuidados Críticos del COVID-19 (FLCCC, en inglés), una organización de médicos de todo el mundo que aboga por el uso de la ivermectina para tratar el COVID-19.
El grupo afirma que la ivermectina, un fármaco antiparasitario aprobado por la FDA que ha tratado la ceguera de los ríos, la sarna y los piojos de la cabeza en los seres humanos, es eficaz para tratar el COVID-19 cuando se utiliza de forma temprana. Se ha demostrado que las propiedades antivirales y antiinflamatorias del fármaco detienen la replicación del virus del PCCh (Partido Comunista Chino), también conocido como nuevo coronavirus, que causa el COVID-19.
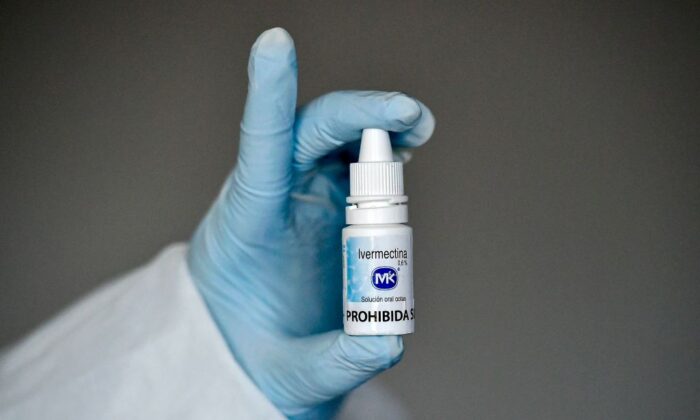
Marik y su organización dijeron que un metaanálisis de 18 ensayos controlados aleatorios mostró que la ivermectina redujo significativamente «la mortalidad, el tiempo de recuperación clínica y el tiempo de eliminación viral» en pacientes con COVID-19. Y en un metaanálisis revisado, que excluye un estudio del que se habían retractado, Marik afirma que los resultados siguen siendo positivos.
«Recientemente, el estudio realizado por Elgazzar et al ha sido objeto de escrutinio con acusaciones de mala praxis científica. Se retractaron de su artículo aparentemente sin su conocimiento y sin darle la oportunidad de defender estos delitos graves», escribió Marik en el American Journal of Therapeutics.
«Mientras se resuelve esta cuestión, decidimos rehacer los metaanálisis originales excluyendo este estudio. Las estimaciones puntuales resumidas no se vieron afectadas en gran medida cuando se eliminó el estudio de Elgazzar et al».
Al igual que el plasma de convaleciente, los NIH no recomiendan ni a favor ni en contra del uso de la ivermectina para tratar el COVID-19, alegando que no hay pruebas suficientes. Pero, a diferencia del plasma de convalecencia, la ivermectina no está aprobada ni autorizada para su uso de emergencia por la FDA, a pesar de las pruebas que demuestran que el fármaco puede tratar varias etapas del COVID-19, y reducir la muerte y la hospitalización.
En las orientaciones actualizadas, la FDA afirma que «los datos actualmente disponibles no demuestran que la ivermectina sea eficaz contra el COVID-19» y advierte a las personas que no deben tomar grandes dosis del fármaco ni utilizar el medicamento destinado a los animales.
La FDA afirma que el método más eficaz para «limitar la propagación del COVID-19» es vacunarse y seguir las orientaciones de los CDC.
Remdesivir sigue siendo el único fármaco antiviral aprobado para pacientes hospitalizados gravemente enfermos con un efecto mínimo. El fármaco se aprobó en octubre de 2020, aunque los resultados de su eficacia para reducir la mortalidad o el tiempo de recuperación fueron dispares.
La Cruz Roja suspende su programa de plasma de convalecientes
La Cruz Roja Americana, dice que había dejado de recolectar plasma de convaleciente de pacientes recuperados de COVID-19 desde junio de 2021 debido a la baja demanda de los hospitales y a que las industrias de la sangre tienen suficiente suministro en el almacén.
«Debido a la disminución de la demanda de los hospitales y porque la Cruz Roja y nuestros socios de la industria han sido capaces de construir un suministro suficiente de plasma de convaleciente para satisfacer las necesidades de los pacientes de COVID-19, la Cruz Roja dejó de recolectar y etiquetar productos de plasma de convaleciente el 14 de junio de 2021», dijo un portavoz de la Cruz Roja a The Epoch Times en un correo electrónico.
Antes de suspender su programa de plasma de convaleciente, la Cruz Roja y otras organizaciones de donación de sangre recibieron instrucciones de la FDA (tras la puesta en marcha de las vacunas) de no recoger plasma de personas vacunadas, a menos que tuvieran la enfermedad y se recuperaran antes de recibir la vacuna.
El portavoz dijo que esto se debía a que «cuando un individuo ha sido infectado por un virus, produce anticuerpos contra múltiples regiones de un virus, incluida la proteína de nucleocápside. Un individuo que haya recibido la vacuna contra el COVID-19 producirá anticuerpos contra la proteína de espiga del virus, pero no contra la proteína de nucleocápside, lo que solo ocurrirá en caso de infección por el COVID-19».
Aunque la Cruz Roja ha suspendido su programa de plasma de convaleciente, la organización afirma que las personas pueden seguir donando sangre o plaquetas independientemente de si se han recuperado del COVID-19 o han recibido la vacuna contra el COVID-19. La Cruz Roja se enfrenta a una escasez de sangre como resultado de la disminución de personas que donan durante la pandemia.
«La Cruz Roja agradece la generosidad del público durante la pandemia, ya que muchos han puesto su empeño en donar sangre que salva vidas para ayudar a los pacientes», dijo el portavoz. «Sin embargo, la Cruz Roja sigue teniendo una necesidad continua y crítica de sangre para salvar vidas, ya que la distribución de productos sanguíneos a los hospitales sigue siendo mayor de lo previsto».
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.