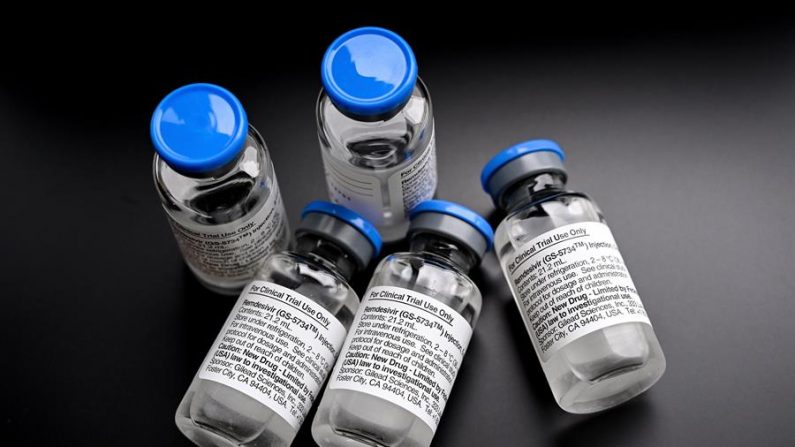
La terapia con remdesivir, una terapia antiviral experimental que se ha utilizado para tratar COVID-19, no tiene un efecto sustancial en las posibilidades de supervivencia de un paciente, según encontró un estudio de la Organización Mundial de la Salud (OMS).
El medicamento antiviral, desarrollado por la farmacéutica estadounidense Gilead Sciences, fue uno de varios medicamentos utilizados para tratar al presidente Donald Trump, luego de su diagnóstico del virus del PCCh (Partido Comunista Chino), a principios de este mes. Remdesivir es uno de los primeros medicamentos en ser utilizado como tratamiento para COVID-19, la enfermedad causada por el virus SARS-CoV-2.
El muy esperado ensayo «solidarity» de la OMS examinó los efectos del remdesivir y de otros tres posibles regímenes de medicamentos, incluida la hidroxicloroquina, la combinación de fármacos anti-VIH lopinavir/ritonavir e interferón, en 11,266 pacientes adultos, en más de 30 países.
El ensayo encontró que los cuatro regímenes «parecían tener poco o ningún efecto sobre los hospitalizados» en la reducción de la duración de la estancia hospitalaria o en la necesidad de ventilar a los pacientes.
“Estos regímenes de Remdesivir, Hidroxicloroquina, Lopinavir e Interferón parecían tener poco efecto sobre la mortalidad hospitalaria”, encontró el estudio.
La OMS dijo el jueves que su estudio también encontró que todos los tratamientos parecían tener poco o ningún efecto sobre la mortalidad a 28 días o durante la hospitalización de los pacientes. El estudio aún no ha sido revisado por pares.
Remdesivir se desarrolló por primera vez como un tratamiento para el ébola y actúa interrumpiendo la capacidad del virus para replicarse.
«Somos conscientes de que los datos iniciales del ensayo SOLIDARITY de la Organización Mundial de la Salud (OMS) se han hecho públicos antes de su publicación en una revista revisada por pares», dijo Gilead al Financial Times en un comunicado.
“Los datos emergentes parecen inconsistentes con evidencia más sólida de múltiples estudios controlados aleatorizados que validan el beneficio clínico del remdesivir”.
«Nos preocupa que los datos de este ensayo global abierto no se hayan sometido a la revisión rigurosa necesaria para permitir una discusión científica constructiva, especialmente dadas las limitaciones del diseño del ensayo».
Daniel O’Day, presidente y director ejecutivo de Gilead Sciences, dijo en una carta abierta el 8 de octubre que, según un estudio de fase 3 controlado con placebo, dirigido por el Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID) de EE.UU. y que cubrió aproximadamente 1060 pacientes hospitalizados en todo el mundo, los pacientes que recibieron remdesivir se recuperaron cinco días más rápido en promedio, y en pacientes con enfermedad grave, siete días más rápido.

El tratamiento también redujo la probabilidad de que los pacientes progresaran a etapas más graves de la enfermedad en las que necesitarían soporte de oxígeno, descubrió el estudio, dijo O’Day.
“En el grupo más grande de pacientes del estudio, los que recibieron oxígeno de bajo flujo, hubo una reducción significativa de la mortalidad en un análisis post-hoc. En la población general, los resultados mostraron una tendencia a la reducción de la mortalidad”, agregó.
La OMS no respondió de inmediato a una solicitud de comentarios de The Epoch Times.
El 1° de mayo, la Administración de Alimentos y Medicamentos (FDA) otorgó la autorización de uso de emergencia al remdesivir, y desde entonces su uso ha sido aprobado o autorizado para tratar el COVID-19 en más de 50 países en todo el mundo.
El presidente comenzó la terapia con remdesivir el 2 de octubre, poco después de su diagnóstico de COVID-19. El médico de la Casa Blanca, el Dr. Sean Conley, dijo en un memorando en ese momento que la terapia antiviral experimental se eligió «en consulta con especialistas».
El presidente también atribuyó su recuperación a un tratamiento experimental de cóctel de anticuerpos de Regeneron Pharmaceuticals Inc. Trump pudo obtener el tratamiento a través de una exención de «uso compasivo».
El cóctel de anticuerpos policlonales antivirales de Regeneron incluye una colección de anticuerpos producidos por las células B. La seguridad y eficacia del fármaco aún no se ha verificado mediante ensayos clínicos.
Mimi Nguyen Ly contribuyó a este artículo.
Con información de Reuters.
Apoye nuestro periodismo independiente donando un «café» para el equipo.
A continuación
Nueve Comentarios Parte 9. La naturaleza criminal del Partido Comunista chino
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.