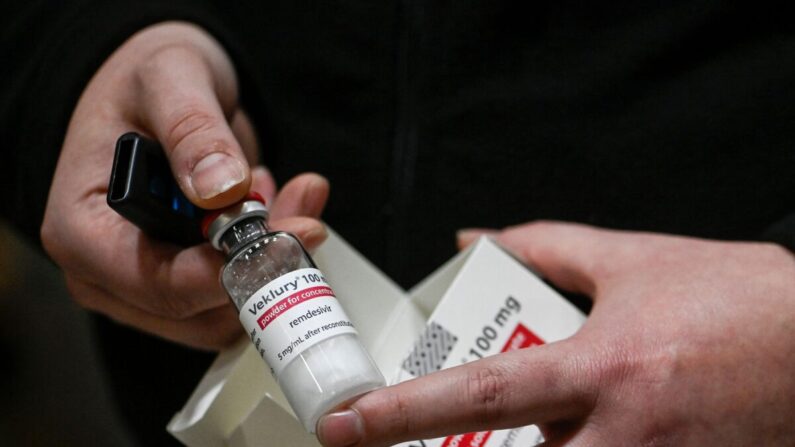
Algunos pacientes que buscan tratamiento fuera de los hospitales pueden ahora utilizar el antiviral remdesivir, después de que los reguladores de medicamentos de Estados Unidos ampliaran la aprobación del fármaco la noche del viernes.
La Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) dijo que la medida se basaba en un estudio realizado por Gilead Sciences, que ha desarrollado el remdesivir, en el que se mostraba que el medicamento reducía el riesgo de hospitalización en un 87% entre las personas que daban positivo en la prueba del COVID-19.
La FDA no citó ninguna otra investigación.
El estudio se realizó antes de que la variante ómicron del virus del PCCh (Partido Comunista Chino) se convirtiera en la predominante en Estados Unidos, aunque el Panel de Directrices de Tratamiento de COVID-19, convocado por los Institutos Nacionales de Salud, afirmó recientemente (pdf) que se espera que el fármaco «sea eficaz contra ómicron».
El panel recomendó que el remdesivir se convirtiera en una opción para los pacientes no hospitalizados junto con el tratamiento de anticuerpos monoclonales ya disponible, el sotrovimab, de GlaxoSmithKline.
Los anticuerpos monoclonales requieren una infusión intravenosa única, frente a la administración intravenosa durante tres días seguidos de remdesivir.
El Dr. David Boulware, especialista en enfermedades infecciosas de la Universidad de Minnesota que estudia los tratamientos contra el COVID-19, señaló en un posteo en las redes sociales que el estudio de Gilead era pequeño —se inscribieron 562 personas, de las cuales aproximadamente la mitad recibieron un placebo— y que un estudio controlado aleatorio de seguimiento probablemente descubriría que es menos eficaz contra la hospitalización.
El remdesivir tampoco redujo la carga viral de los pacientes, a diferencia de las píldoras para el COVID-19 de Pfizer y Merck, otras dos opciones de tratamiento, señaló.
La medida de la FDA significa que las personas de 12 años o más que pesen al menos 88 libras, que hayan dado positivo en la prueba de COVID-19, que no estén hospitalizadas y que se consideren en alto riesgo de evolucionar a COVID-19 grave pueden ahora obtener el medicamento, que antes estaba restringido a los pacientes hospitalizados.
La FDA también ha autorizado el fármaco para los niños menores de 12 años que pesen al menos 3.5 kilogramos (7.7 libras) y cumplan los mismos criterios.
«Las acciones de hoy proporcionan a los adultos y a los pacientes pediátricos, con COVID-19 de leve a moderada y con un alto riesgo de COVID-19 grave, una opción de tratamiento que podrían recibir fuera de un entorno hospitalario tradicional, incluso en establecimientos con enfermeras debidamente capacitadas, en entornos de atención sanitaria a domicilio y en instalaciones para pacientes externos, como los centros de infusiones», dijo en un comunicado la Dra. Patrizia Cavazzoni, directora del Centro de Evaluación e Investigación de Medicamentos de la FDA.
La autorización ampliada «proporciona el visto bueno de la FDA a lo que ya se está haciendo para suplir las limitaciones de suministro de otros productos terapéuticos. Por lo tanto, es algo bueno», dijo a The Epoch Times el Dr. David Wohl, profesor del Instituto de Salud Global y Enfermedades Infecciosas de la Universidad de Carolina en Chapel Hill, en un correo electrónico.
Wohl, que ha recibido financiación de Gilead, ha estudiado el remdesivir y ha descubierto que ayuda a prevenir la muerte.
Otros estudios también han demostrado que «el remdesivir también es eficaz en las primeras fases de la infección por COVID-19, además de ayudar a los pacientes que están hospitalizados con la enfermedad», dijo el director ejecutivo de Gilead, Daniel O’Day, en un comunicado de prensa.
Por otra parte, algunas investigaciones sobre el remdesivir, el primer fármaco aprobado contra el COVID-19 en Estados Unidos, han obtenido resultados contradictorios. Por ejemplo, un estudio publicado en The Lancet el año pasado no encontró ningún beneficio clínico entre los pacientes gravemente enfermos que fueron ingresados en hospitales.
Además, varios estudios han concluido que los trastornos renales son uno de los efectos secundarios de los fármacos, y la etiqueta de remdesivir (pdf) dice que se observaron problemas renales en las pruebas realizadas en animales.
Según la etiqueta, las personas que planean recibir el medicamento, también conocido como Veklury, deben informar a su proveedor de atención médica si tienen problemas renales o hepáticos antes de recibirlo.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.