En una decisión sin precedentes, un juez de Michigan dictaminó el 8 de agosto que un fabricante de medicamentos y un hospital no están protegidos por la Ley de Preparación Pública ante Emergencias (PREP) en el caso de un hombre que sufrió dos derrames cerebrales y la amputación de una pierna tras recibir el medicamento para COVID-19 remdesivir que estaba contaminado con partículas de vidrio.
Esta es la primera vez que un juez dictamina que un fabricante de medicamentos y un hospital no están protegidos por la Ley PREP, que proporciona inmunidad frente a demandas y protecciones de responsabilidad en virtud de la legislación estatal y federal en relación con todas las reclamaciones por pérdidas derivadas de la administración de la contramedida cubierta, salvo en caso de conducta dolosa. Aunque la sentencia no es un precedente vinculante, este caso marca la pauta para futuras demandas contra la empresa por lesiones en las que puedan incurrir las personas a las que se administre el medicamento.
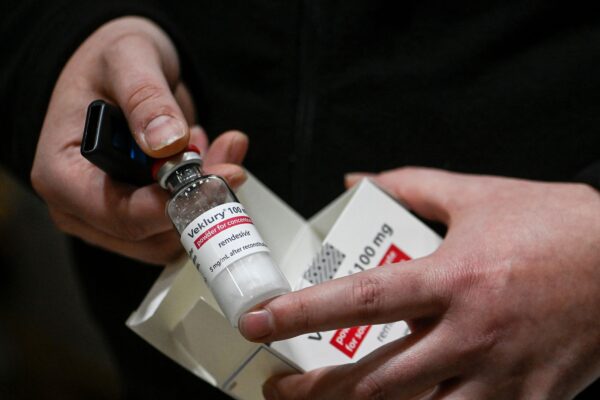
El abogado Ven Johnson, de Detroit, presentó una demanda en nombre de Dan Nowacki, su esposa y su hijo contra Gilead Sciences, Inc. (Gilead), fabricante de remdesivir —comercializado bajo la marca Veklury— y el hospital St. Joseph Mercy Chelsea, que administró el fármaco, alegando incumplimiento de garantía, negligencia, negligencia grave y pérdida de consorcio, ya que la Sra. Nowacki ha perdido la «sociedad, compañía y servicios domésticos» de su marido.
El hospital y la empresa farmacéutica alegaron que no podían ser demandados porque gozaban de inmunidad en virtud de la Ley PREP.
«Su argumento ha sido: ‘Sí, sabemos que lo retiramos voluntariamente. Sí, sabemos que contiene partículas de vidrio, y sabemos que se administraron dos dosis a Dan, y sabemos que tuvo un derrame cerebral. Pero como seguimos las directrices de la FDA y fuimos aprobados, tenemos inmunidad farmacéutica. No pueden demandarnos porque fue aprobado por la FDA'», declaró Johnson a The Epoch Times.
«Obviamente, cuando presentamos el caso sabíamos que impugnar la inmunidad que otorga la Ley PREP sería una ardua batalla», declaró el Sr. Johnson. «Pero no podríamos estar más orgullosos de que ambos jueces [en el tribunal estatal y federal] vieran a través de la farsa: que Gilead Sciences Inc. obtuvo la aprobación para el medicamento, pero no para las partículas de vidrio».
Según la denuncia (pdf) obtenida por The Epoch Times, el Sr. Nowacki ingresó el 10 de noviembre de 2021 en el hospital St. Joseph Mercy Chelsea y se le diagnosticó COVID-19. Durante su estancia, recibió cinco dosis de remdesivir. Al menos dos dosis pertenecían a lotes contaminados.
Días después, el Sr. Nowacki sufrió su primer infarto cerebral masivo. El 24 de noviembre, el Sr. Nowacki fue dado de alta en un centro de enfermería especializada y empezó a desarrollar hematomas e hinchazón en las manos, la cara y los brazos. Volvió a ingresar en el hospital Henry Ford, donde sus «síntomas seguían siendo un misterio para los médicos».
El 16 de diciembre, Nowacki sufrió un segundo derrame cerebral que le dejó postrado en cama y con necesidad de cuidados permanentes las 24 horas del día para el resto de su vida.

Remdesivir, autorizado por primera vez por la FDA en mayo de 2020, es un medicamento antivírico que actúa sobre el ARN del SARS-CoV-2 para prevenir su replicación y los síntomas de la enfermedad. Desde entonces se ha aprobado para adultos y niños de hasta 28 días que pesen al menos 6.6 libras.
Según un anuncio de la empresa publicado el 3 de diciembre de 2021 en el sitio web de la FDA, Gilead retiró voluntariamente dos lotes de Veklury, también conocido como remdesivir, tras recibir una queja de un cliente sobre la presencia de partículas de vidrio en el medicamento y confirmar mediante una investigación que la reclamación era cierta.
La empresa admitió en una declaración de riesgos que las «partículas de vidrio» pueden «provocar accidentes cerebrovasculares o incluso causar la muerte» si llegan a los vasos sanguíneos, se desplazan a diversos órganos u obstruyen los vasos sanguíneos del corazón, los pulmones o el cerebro. Sin embargo, Gilead declaró en ese momento que no había recibido ninguna notificación de acontecimientos adversos relacionados con la retirada y que estaba notificando a sus distribuidores y clientes a través de UPS next day air a las farmacias hospitalarias para facilitar la devolución de los viales restantes de los lotes afectados.
Según un comunicado de prensa (pdf) emitido por Ven Johnson Law, la retirada afectaba aproximadamente a 55,000 dosis de remdesivir.
Sin embargo, el Sr. Nowacki y su familia no fueron notificados de la retirada hasta que el hospital St. Joseph Mercy envió una carta (pdf) cuatro meses después, en abril de 2022, confirmando que el Sr. Nowacki había recibido al menos dos dosis de remdesivir de lotes potencialmente contaminados con partículas de vidrio. El Sr. Johnson también dijo que sus clientes fueron los primeros en ponerse en contacto con Gilead y el hospital para preguntar si el Sr. Nowacki había recibido remdesivir de lotes contaminados. Gilead dijo que tenían que ponerse en contacto con el hospital.
«Una de las cosas que vamos a averiguar es qué sabían exactamente Gilead, la FDA y el hospital, y cuándo», declaró Johnson a The Epoch Times. «¿Cómo llegaron a este medicamento partículas de vidrio que podrían causar derrames cerebrales y la muerte de personas? ¿Por qué estas personas no se dirigen a nosotros para obtener los historiales médicos de nuestro cliente y entender lo que ocurrió?».
El Sr. Johnson dijo que no entendía por qué Gilead no hizo esfuerzos para ponerse en contacto con las personas que potencialmente habían recibido los lotes contaminados o ayudar a los que pueden haber sido perjudicados, sino que están tratando de esconderse detrás de tecnicismos.
«El caso de Dan Nowacki es un trágico ejemplo de las devastadoras consecuencias que pueden derivarse de la pura negligencia y avaricia de las empresas farmacéuticas y de la incompetencia del St. Joseph Mercy Chelsea al no avisar a tiempo de la retirada de un medicamento», declaró el Sr. Johnson, en un comunicado de prensa. «Los fabricantes de medicamentos y las instituciones médicas deben dar prioridad a la seguridad de los pacientes por encima de todo. El retraso de cuatro meses en avisar a Nowacki de la retirada del remdesivir impidió a los posteriores tratantes del Sr. Nowacki administrarle el tratamiento necesario, lo que comprometió la recuperación de Nowacki.»
El Sr. Johnson declaró a The Epoch Times que no es habitual que una empresa emita una retirada voluntaria.
«Tuvieron que haber tenido contacto con la FDA», dijo. «Afirman en su comunicado de prensa de diciembre que tenían pruebas de un cliente que había tenido algún tipo de reacción, y confirmaron que era exacto, pero cuándo fue, dónde ocurrió y cuándo se enteraron por primera vez, porque este proceso no ocurrió en dos o tres semanas».
Ahora que un juez determinó que Gilead y el hospital no gozan de inmunidad en virtud de la Ley PREP, el siguiente paso es la presentación de pruebas, seguida de un juicio.
El Sr. Johnson está animando a la Fiscal General de Michigan, Dana Nessel, a investigar cómo se comercializó el medicamento en su estado y anima a cualquiera que tenga información sobre cómo las partículas de vidrio acabaron en el medicamento o que también pueda haber recibido dosis contaminadas a ponerse en contacto con su bufete de abogados.
The Epoch Times se puso en contacto con Gilead Sciences, Inc. y con el hospital St. Joseph Mercy Chelsea para obtener comentarios sobre el litigio pendiente y no recibió respuesta al cierre de esta edición.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.