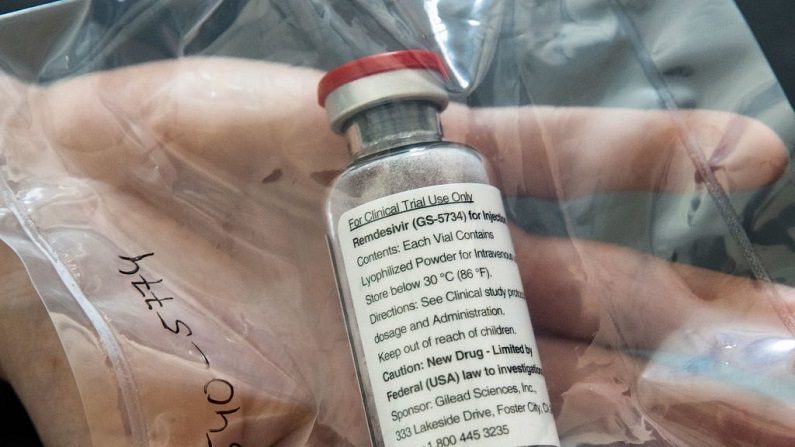
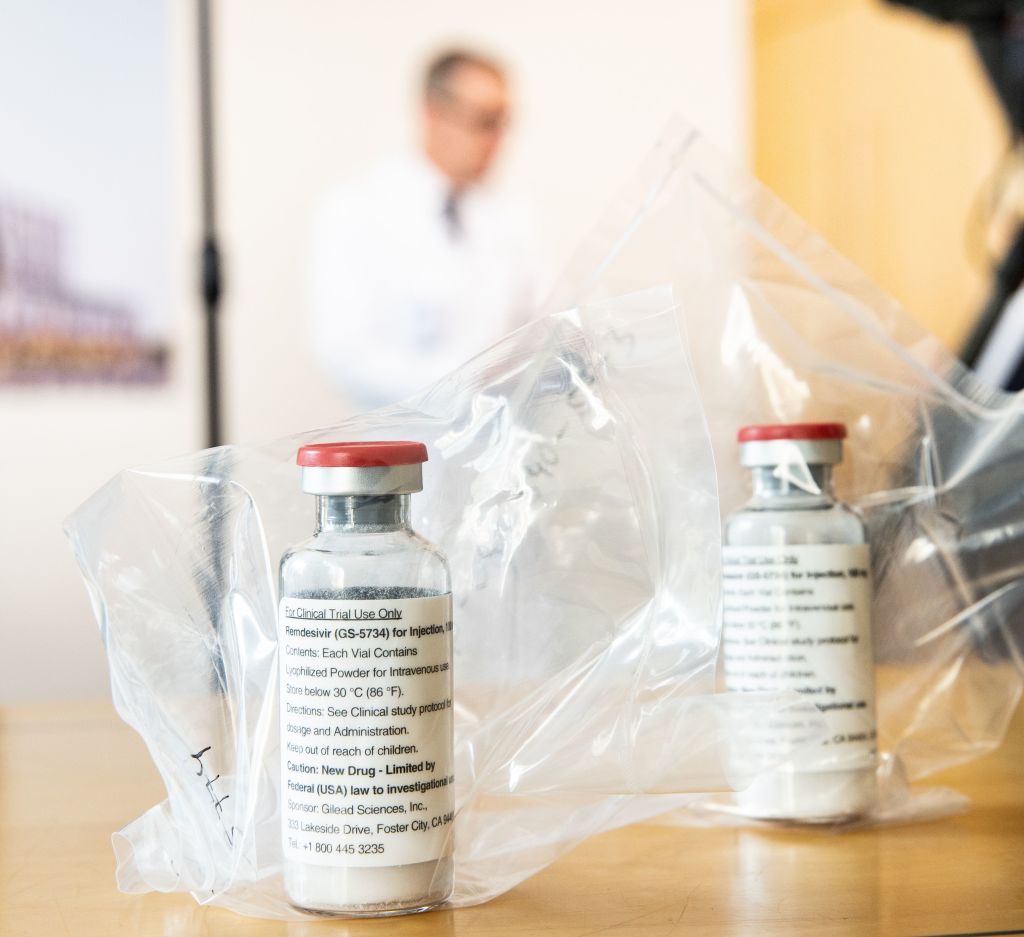
Los datos revisados por expertos de un estudio impulsado por las autoridades de salud muestran que el remdesivir aceleró la recuperación de COVID-19, pero los investigadores dijeron que el medicamento requiere un suplemento y mostró poco beneficio en muchos grupos de pacientes.
Los datos muestran que el medicamento experimental acortó el tiempo promedio de recuperación de 15 a 11 días. A un grupo se le administró un tratamiento de 10 días de remdesivir por vía intravenosa, mientras que a otro se le dio un tratamiento estándar y un placebo.
El ensayo aleatorio a doble ciego incluyó a 1063 pacientes en 10 países.
«Los resultados preliminares de este estudio sugieren que un ciclo de 10 días de remdesivir fue superior al placebo en el tratamiento de pacientes hospitalizados con COVID-19», escribieron los investigadores en el New England Journal of Medicine.
Los resultados son preliminares porque una junta independiente de supervisión de datos y seguridad recomendó que se desenmascararan los resultados después de que un análisis mostrara que remdesivir aceleraba la recuperación de COVID-19, la enfermedad causada por el virus del PCCh (Partido Comunista Chino). No está claro si el ensayo continúa.
Los investigadores observaron una alta tasa de mortalidad en los pacientes a pesar del uso de remdesivir.
«Estos hallazgos preliminares respaldan el uso de remdesivir en pacientes que están hospitalizados con COVID-19 y requieren terapia de oxígeno suplementario», con el mayor beneficio observado entre los pacientes que necesitaban suplemento de oxígeno pero no estaban ventilados mecánicamente, dijo el equipo, que fue dirigido por científicos del Instituto Nacional de Alergia y Enfermedades Infecciosas (NIAID).
«Sin embargo, dada la alta mortalidad a pesar del uso de remdesivir, es evidente que el tratamiento con un medicamento antiviral por sí solo probablemente no sea suficiente. Las estrategias futuras deberían evaluar los agentes antivirales en combinación con otros enfoques terapéuticos o combinaciones de agentes antivirales para seguir mejorando los resultados de los pacientes con COVID-19».
Un estudio iniciado a principios de este mes está evaluando el remdesivir con baricitinib, un medicamento antiinflamatorio, en comparación con el remdesivir solo.
El tratamiento debe comenzar antes de que la progresión de COVID-19 avance tanto que los pacientes necesiten ayuda para respirar, según los nuevos hallazgos.
Reacciones
Zain Chagla, médico de enfermedades infecciosas de St. Joseph’s Healthcare Hamilton en Toronto, dijo que el estudio mostró que ningún grupo se recuperó más rápido excepto los pacientes que necesitaban oxígeno suplementario.
«En resumen: si vienes al hospital y necesitas un poco de oxígeno, esta droga puede llevarte a casa más rápido. Pero en algunas personas, el riesgo de morir es muy pequeño si se entra en esa categoría (en algunos estudios es del 0 por ciento). Esto no es un cambio de juego. Es un ensayo negativo», dijo en una declaración.
Eric Topol, fundador y director del Instituto Translacional de Investigación Scripps, dijo a STAT News que el estudio muestra que el remdesivir es «un medicamento muy seguro y efectivo», aunque no hubo señales de mejora en los pacientes con los casos más graves.
«Ahora tenemos un primer medicamento eficaz definitivo para COVID-19, que es un gran paso adelante y se construirá sobre la base de otros medicamentos [ y] combinaciones de medicamentos», dijo.
Los resultados iniciales del ensayo se publicaron el mes pasado y fueron promocionados rápidamente por los funcionarios de salud, incluido el jefe del NIAID, el Dr. Anthony Fauci, quien dijo que remdesivir «tiene un claro y significativo efecto positivo en la disminución del tiempo de recuperación».
Aunque surgieron preguntas sobre el punto final que se modificó durante el ensayo, la Administración de Alimentos y Medicamentos autorizó el uso de emergencia de remdesivir para tratar a pacientes con el virus del PCCh y los funcionarios federales de salud comenzaron a distribuir dosis donadas por el fabricante Gilead Sciences a más de una docena de estados.
Los hallazgos sobre la mortalidad no fueron lo suficientemente significativos desde el punto de vista estadístico, señalaron los investigadores, pero sugirieron un beneficio de supervivencia, con una tasa de mortalidad de 7.1 por ciento para los que recibieron remdesivir frente a 11.9 por ciento del grupo placebo.
Cuarenta y nueve pacientes tuvieron que suspender el tratamiento con remdesivir antes del día 10 debido a un evento adverso o porque se retiraron, dijeron los investigadores. Los eventos adversos graves ocurrieron en 21.1 por ciento en el grupo de remdesivir y en 141 pacientes, o 27 por ciento, en el grupo placebo.
Gilead, con sede en California, respondió positivamente a los resultados.
«Estos hallazgos respaldan el uso de remdesivir en esta población, con el mayor beneficio observado entre los individuos que requerían suplementos de oxígeno pero no estaban ventilados mecánicamente», dijo en una declaración el Dr. Merdad Parsey, director médico de Gilead.
La compañía espera que los resultados de un estudio de fase tres separado se publiquen pronto.
Siga a Zachary en Twitter: @zackstieber
Apoye nuestro periodismo independiente donando un «café» para el equipo.
A continuación
La subversión comunista china de la OMS socavó la respuesta a la pandemia
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.