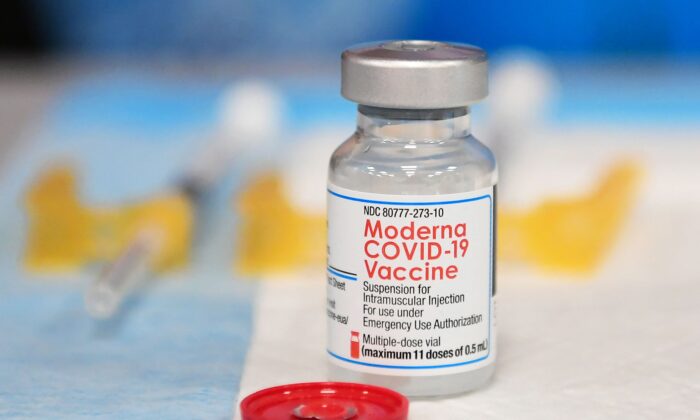
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó el lunes la vacuna anti-COVID de Moderna para todos los estadounidenses mayores de 18 años, a pesar de que la vacuna brinda poca protección contra la enfermedad desde la aparición de la variante ómicron.
La FDA dijo que la vacuna tuvo una efectividad del 93 por ciento en la prevención del virus del PCCh (Partido Comunista Chino), que causa el COVID-19 y que es conocido como SARS-CoV-2.
No obstante, los datos que se analizaron, que también mostraron que la vacuna tuvo una efectividad del 98 por ciento en la prevención de enfermedades graves, se recopilaron antes de la aparición de ómicron.
La variante relativamente nueva evita fácilmente la protección de la vacuna de Moderna y de las otras dos vacunas contra el COVID-19 que se usan en Estados Unidos, según estudios y datos del mundo real, incluida una investigación reciente respaldada por los Centros para el Control y la Prevención de Enfermedades (CDC).
El Dr. Peter McCullough, cardiólogo, le dijo a The Epoch Times en un correo electrónico que la aprobación “no es clínicamente justificable ni está respaldada por datos clínicos”.
“Necesitaríamos un gran ensayo aleatorizado en pacientes con ómicron con el resultado compuesto de hospitalizaciones y muertes. Dado el perfil de seguridad muy deficiente de las vacunas COVID-19, claramente necesitaríamos una relación positiva de beneficio-riesgo antes de que estas vacunas puedan adoptarse en la práctica clínica. Dada la naturaleza leve de ómicron y su fácil manejo, es poco probable que alguna vacuna tenga un papel para esta variante”, agregó.
El Dr. Thomas Russo, jefe de la División de Enfermedades Infecciosas del Departamento de Medicina de la Escuela Jacobs de Medicina y Ciencias Biomédicas de la Universidad de Buffalo, no está de acuerdo.
“Tenemos una gran cantidad de datos que respaldan que el beneficio es significativo y extraordinariamente seguro”, le dijo a The Epoch Times. “De hecho, estoy un poco sorprendido de que haya tardado tanto, pero parece que la FDA hizo todo lo posible para asegurarse de que todo estuviera en orden”.
Los portavoces de la FDA no respondieron de inmediato a las solicitudes de comentarios.
La FDA dijo que el paquete que analizó incluía datos preclínicos y clínicos de un ensayo de fase 3 en el que se les hizo seguimiento a unos 15,000 receptores de la vacuna y que se utilizó para apoyar la autorización de uso de emergencia de la agencia a la misma vacuna, en diciembre de 2020.
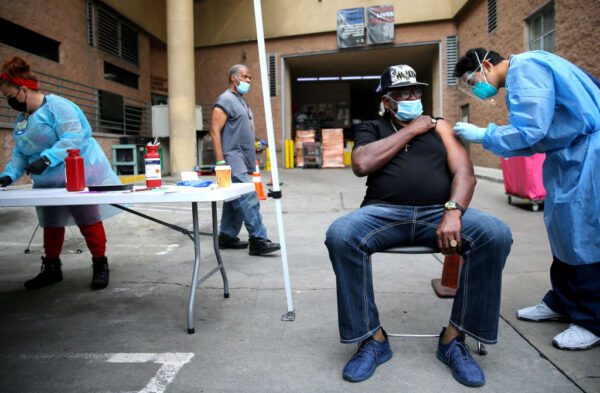
La agencia analizó los datos para determinar si la vacuna cumplía con los estándares para su aprobación.
La vacuna aprobada se comercializará como Spikevax. Tiene la misma formulación que la vacuna autorizada y se puede usar indistintamente con la inyección autorizada, según la FDA. Spikevax fue aprobada previamente en muchos otros países, incluidos Canadá, Israel y Japón.
“El público puede estar seguro de que Spikevax cumple con los altos estándares de seguridad, eficacia y calidad de fabricación de la FDA requeridos para cualquier vacuna aprobada para su uso en Estados Unidos”, dijo en un comunicado la Dra. Janet Woodcock, directora interina de la agencia.
“Los expertos médicos y científicos de la FDA realizaron una evaluación exhaustiva a los datos e información científica incluida en la solicitud relativa a la seguridad, la eficacia y la calidad de fabricación de Spikevax”, añadió el Dr. Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA.
La aprobación es sólo para la serie primaria de Moderna, que consiste en dos inyecciones que se aplican con una diferencia aproximada de un mes.
La serie primaria es de poco beneficio en términos de protección contra infecciones desde que ómicron se convirtió en la cepa dominante, según la investigación sobre los efectos de la variante. Los funcionarios federales de salud recomiendan que las personas reciban un refuerzo de Moderna cinco meses después de su segunda inyección para obtener una mejor protección contra el virus del PCCh.
La reciente aprobación asignada a la vacuna de Moderna es la segunda de su tipo tras la aprobación, por parte de la FDA, a la vacuna de Pfizer en agosto de 2021.
Stéphane Bancel, CEO de Moderna, dijo que la aprobación fue «un hito trascendental en la historia de Moderna, ya que es nuestro primer producto en obtener la licencia en EE.UU.».
“Agradecemos a la FDA de EE.UU. por su revisión exhaustiva a nuestra solicitud. Nos sentimos honrados por el papel que está desempeñando Spikevax para ayudar a poner fin a esta pandemia”, agregó.
Únase a nuestro canal de Telegram para recibir las últimas noticias al instante haciendo click aquí
Cómo puede usted ayudarnos a seguir informando
¿Por qué necesitamos su ayuda para financiar nuestra cobertura informativa en Estados Unidos y en todo el mundo? Porque somos una organización de noticias independiente, libre de la influencia de cualquier gobierno, corporación o partido político. Desde el día que empezamos, hemos enfrentado presiones para silenciarnos, sobre todo del Partido Comunista Chino. Pero no nos doblegaremos. Dependemos de su generosa contribución para seguir ejerciendo un periodismo tradicional. Juntos, podemos seguir difundiendo la verdad.